《新疆医学》2022年8月第52卷 第8期
普萘洛尔联合聚桂醇治疗血管瘤的临床观察
范琴,王树坚,李娜,黎毅,姚艳,王其恩
摘要:
目的:评价普萘洛尔联合聚桂醇局部注射治疗婴儿血管瘤的临床疗效及不良反应。
方法:采集2018年6月-2020年7月于我科住院治疗的血管瘤患儿39例,采取口服普萘洛尔联合聚桂醇局部注射治疗,治疗后同时随访观察6个月。
结果:普萘洛尔联合聚桂醇局部注射治疗婴儿血管瘤总有效率为88.6%,在治疗部位方面,头面颈部、四肢关节及会阴部位的治疗有效率无显著差异(P>0.05)。聚桂醇局部注射的不良反应为局部渗血及肿胀,普萘洛尔口服过程中的不良反应为低血压、心率减慢及肢端发冷。
结论:对于一些特殊类型的血管瘤,采用普萘洛尔联合聚桂醇的治疗方法较单一的治疗方法疗效更快,疗程短。
关键词:
婴儿血管瘤;普萘洛尔;聚桂醇
婴儿期血管良性肿瘤可分为婴儿血管瘤(Infantile hemangioma)、先天性血管瘤(congenital hemangioma)、分叶状毛细血管瘤(Lobular capillary hemangioma)等多种类型,其中以IH最常见。国外报道IH发病率在4%-5%左右,国内发病率较国外稍低[1-3]。而未经治疗的血管瘤患儿中有超过50%的报道会产生疤痕、萎缩、增生、变色和毛细血管扩张等[4]。因此临床上通常建议提早干预。增殖期的IH,主要的治疗手段包括激光、局部外用药、局部注射、口服药物及手术治疗。2008年Léauté-Labrèze医生首先在全世界报道了口服普萘洛尔治疗血管瘤,开创了普萘洛尔治疗IH的先河[5]。现将我科2018年6月-2020年7月39例采用普萘洛尔联合聚桂醇局部注射治疗婴儿血管瘤的临床总结汇报如下:
一、资料与方法
1.1 一般资料
研究对象为2018年6月-2020年12月30例我科的IH住院患儿,患儿年龄在62 d至6岁,患儿血管瘤面积为16 mm×15 mm-110 mm×110 mm。瘤体位置在头面、颈部、关节、会阴等特殊部位,以及包括在躯干、四肢的较大深在性的血管瘤。所有IH均未接受治疗,在彩超下显示瘤体>10 mm。
1.2用药前检查及知情同意
所有患儿在治疗前均行常规肝肾功能、心肌酶、血、尿、便,腹部彩超、胸片、心电图等常规检查。同时排除窦性心动过缓、II度以上房室传导阻滞、低血压等其他心脏疾病以及支气管哮喘、肺炎等肺部疾病。治疗前签署知情同意书,同时告知可能出现的相关不良反应,家属及其监护人签字同意后进行。治疗后每周检测血压、心率、呼吸,每月复查血糖、心血管功能相关指标。治疗前均对监护人进行健康科普教育,告知在治疗过程中可能出现的不良反应,并嘱家属进行密切观察,如出现相应的不良反应均及时报告。
1.3 治疗方法
患儿检查结果无异常后予以普萘洛尔(心得安)口服,第一天总药量为0.5 mg/kg,第二天总药量为0.75 mg/kg,第三天药量为1.0 mg/kg,第四天药量为1.5mg/kg,每天总药量分早晚两次用5%葡萄糖10ml溶解后注射器抽取口服。最大剂量为2 mg/kg。无特殊不良反应的情况下在服药第四天进行聚桂醇(陕西天宇制药有限公司)注射治疗。注射均采取泡沫注射Tessari法[6],具体方法是通过一个三通管连接两个10 ml的注射器,一个注射器抽取1 ml聚桂醇原液,另一注射器抽取4 ml空气,在三通管内迅速进行20次推注产生泡沫。泡沫制作完成后用5号头皮针连接2个装好泡沫的注射器以及2个空注射器,在局部彩超的引导下分别在瘤体的上下左右进行穿刺,可见回血时注射泡沫,瘤体发白或注射器均可无阻力推注时快速拔针并用无菌纱布压迫止血。聚桂醇注射治疗后无特殊不良反应间隔1周再次注射。
1.4 观察指标
住院期间着重观察IH患儿不良反应的发生并进行记录。治疗后随访观察6个月,并拍照记录。疗效评判标准为:1级:瘤体体积减少≤25%为无效;2级:瘤体体积减少26%-50%为好转;3级:瘤体体积减少51%-75%为显效;4级:瘤体体积减少76%-100%为治愈。
1.5 统计学处理
本研究的数据均采用SPSS25.0进行处理。计数资料以单位例表示,计数资料的比较采用Fisher确切概率法检验,P<0.05为差异有统计学意义。
二、结果
2.1 临床疗效
最终纳入研究39例患儿,失访1例。39例患儿中,治疗疗效1级为3例,2级为3例,3级为11例,4级为22例。普萘洛尔联合聚桂醇治疗IH总有效率为88.6%,在治疗部位方面,头面颈部、四肢关节及会阴部位的治疗有效率无显著差异(P>0.05)。见表1,部分IH患儿疗效见下图(图1、图2)。
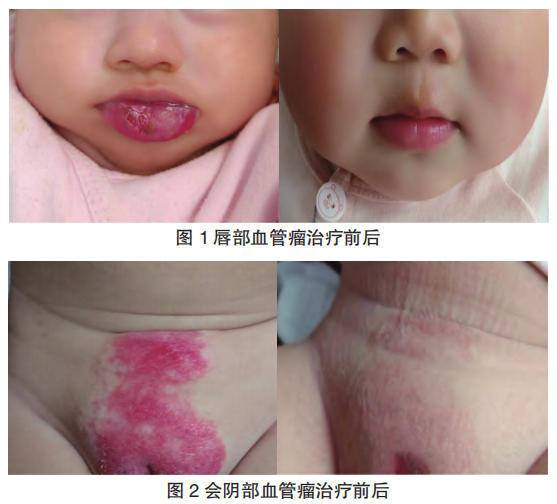
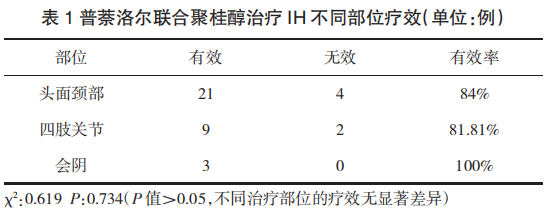
2.2 不良反应
在39例进行治疗的IH患儿中,主要出现的不良反应在于口服普萘洛尔导致。局部注射聚桂醇除注射后注射部位轻微渗血、局部肿胀外无特殊不良反应。出现血压降低15例,心率减慢6例,肢端发凉4例,经过频繁喂养、进食后服药等处理后患儿心率未下降至该年龄段最低心率的70%以下,血压未减低到基准血压的25%以上,因此不影响继续用药。不良反应常出现在口服药物第一周。此外,3例卵圆孔未闭及1例二尖瓣轻度反流患儿在服药期间未出现严重不良心脏反应。
三、讨论
在本研究中,普萘洛尔联合聚桂醇治疗IH疗效好,安全性高,副作用少。无论是对于两个多月的婴儿还是年龄小的儿童,二者联合治疗对婴幼儿而言安全性相对较高。国内外许多文献都有相关<28d婴儿口服普萘洛尔的研究,除对血压、心率、血糖等常见不良反应的研究外,甚至有研究该药对神经发育的影响,结果证明普萘洛尔对儿童神经发育结果没有影响[7]。因此足以证明该药物的安全性。国内户佐珍、王淼、穆细院[8-10]等报道均对1个月以上的婴儿进行聚桂醇单独或联合其他手段治疗血管瘤,疗效及安全性均得以肯定。在副作用方面,39例患儿中,有2例患儿在用药前出现肝功能异常,肝酶升至正常值2倍以上,经消化科会诊评估用药后未出现特殊不良反应,出院后在后续随访及复诊过程中有1例肝酶逐渐降至正常,有1例后续肝酶变化不大,但均不影响用药。另外,4例心脏彩超异常患儿用药中未出现严重不良心脏反应。在本次研究中,局部注射聚桂醇除注射后1-2 d有局部肿胀外几乎无特殊的副作用,文献报道聚桂醇注射后出现色素沉着、神经系统不良事件(如视觉障碍、头疼等)、血栓栓塞、心脏毒性等副作用在本次研究中尚未发生,这可能与本次样本量相对局限,同时严格把握适应症在治疗剂量、操作速度方面有关。而在口服普萘洛尔中,血压降低、心率减慢是最常见的副作用。其他诸如支气管哮喘、呕吐、低血糖、高血钾、精神亢奋等副作用在本次研究中尚未出现。
普萘洛尔治疗血管瘤的完整机制尚不清楚,目前公认它通过阻断血管内皮生长因子和碱性成纤维细胞生长因子的促血管生成信号来阻止IH的生长,在药物作用后期加速异常细胞的凋亡。普萘洛尔在2014年3月已获得美国食品和药物管理局的批准来治疗婴儿血管瘤。单独应用该药物的有效性在国内已得到普遍证实,无论是在少数民族地区还是偏远地区[11]。全身性应用普萘洛尔治疗最常见的副作用包括嗜睡、腹泻、烦躁、四肢发冷、出现皮疹等。其次为支气管痉挛,低血糖,情绪障碍,心动过缓和低血压。但有时也需要警惕该药的一些严重不良反应的发生。国外陆续报道有患儿口服普萘洛尔引起较为严重的罕见并发症—高血钾,最高可达7.3 mmol/L[12-15]。到目前为止,尚无指南建议对婴儿血管瘤患者口服普萘洛尔后应进行血清钾水平检查,临床医生应当提高对此不良反应的重视。聚桂醇治疗IH的原理为其损伤血管内皮细胞,使作用部位的血小板、纤维蛋白、红细胞等沉积形成血栓,从而阻塞血管,另外聚桂醇还使靶血管损伤,血栓纤维化,使其逐渐吸收、缩小至消失。陆晓逸、蔡仁慧等[16-17]应用聚桂醇治疗血管瘤过程中出现的不良反应有糜烂、结痂、一过性干咳、胸闷等,在本次研究中未出现。国内卢国坚、刘召明有报道[18-19]普萘洛尔联合聚桂醇治疗IH较单用普萘洛尔可缩短治疗疗程,近期疗效好。
由于样本局限及其他客观原因,本研究尚未对每一具体部位的血管瘤进行详细分类研究,如唇部血管瘤、口腔内血管瘤、鼻部血管瘤、眼部血管瘤等对其起效时间进行详细观察。另外由于有的患儿尚在随访中,因此对于普萘洛尔停药多久后出现反跳的情况未得出结论。
综上所述,普萘洛尔联合聚桂醇治疗婴儿血管瘤可以提高疗效,且不良反应轻微,值得临床推广应用。但是值得注意的是由于血管瘤具体发表机制尚未明了,二者治疗婴儿血管瘤时应当严格把握适应症、禁忌症及相关操作方法,同时严密随访评估用药量、停药指征等。
参考文献







