发布时间:2021-03-22 16:28:15 来源: 浏览次数:1129
《现代消化及介入诊疗》2021年第26卷第7期
内镜下硬化剂联合组织胶注射在食管胃底静脉曲张早期排胶出血中的临床应用
张震
摘要:
目的:探讨食管胃底静脉曲张破裂出血(esophageal and gastric varices bleeding,EGVB)的内镜下硬化剂联合组织胶止血治疗的临床疗效。
方法:回顾性分析2013年1月至2018年1月辽阳市中心医院采用内镜下硬化剂和(或)组织胶注射治疗的192例EGVB患者,其中A组采用组织胶注射治疗共94例;B组采用硬化剂联合组织胶注射治疗共98例。记录192例基线资料包括:患者性别、年龄,乙肝或酒精性肝硬化情况、Child-Pugh评分、门静脉直径、肝功能、凝血功能以及静脉曲张严重程度。比较分析A组和B组的基线资料及其在早期排胶过程中出血发生率、组织胶用量、异位栓塞发生率的差异性。
结果:A组和B组的性别、年龄、肝功能、凝血功能、门静脉直径及Child-Pugh评分比较,无显著性差异,P>0.05;A组术后排胶出血率为7.45%明显高于B组的1.02%,P<0.05;A组组织胶用量为(32.2±1.7)mL明显高于B组的(4.7±1.2)mL,P<0.05;A组术后异位栓塞发生率为4.26%明显高于B组的2.04%,P<0.05。
结论:内镜下硬化剂联合组织胶注射治疗EGVB显著降低早期排胶出血率和异位栓塞率,临床疗效满意。
关键词:
内镜下硬化注射;组织胶注射;食管胃底静脉曲张破裂出血;内镜
食管胃底静脉曲张破裂出血(esophageal and gastricvarices bleeding,EGVB)是消化内科、急诊科和肝病科之间联合救治的危急重症,受到医护工作者高度重视。内镜下硬化剂、组织胶注射及套扎等方法是目前公认的EGVB最有效的治疗方法[1-2]。临床研究发现:急诊采用组织胶注射法治疗EGVB的止血率高达95%~100%,但组织胶作为异物在体内排出过程中引发的二次出血率也较其他止血方法高,是组织胶注射治疗EGVB主要的并发症[3]。因此,减少早期排胶出血并发症的发生是提高EGVB救治的重要研究课题[4]。本研究分析内镜下硬化剂联合组织胶注射治疗EGVB,为EGVB的内镜治疗提供参考。
一、资料与方法
1.1 一般资料
1.1.1 研究对象
回顾性分析2013年1月至2018年1月辽阳市中心医院采用内镜下组织胶注射治疗EGVB患者94例、内镜下硬化剂联合组织胶注射治疗EGVB患者98例。前者为A组:男55例、女39例,年龄28~76岁,平均年龄(53.6±2.4)岁;后者为B组:男58例、女40例,年龄25~78岁,平均年龄(54.1±1.9)岁。192例患者入院后均进行静脉采血检测血清肝炎病毒标志物(HBsAg、HBsAb、HBeAg、HBeAb、HBcAb)、肝功能(ALT、AST、r-GT、ALB、TBiL、DBIL)、血液常规、凝血功能(血小板计数、凝血酶时间、凝血酶原时间);记录Child-Pugh评分及门静脉治疗前后的直径变化。
1.1.2 入组标准
①符合《肝硬化门静脉高压症食管、胃底静脉曲张破裂出血诊治专家共识》中关于EGVB的诊断标准[1-2];②无内镜检查禁忌症;③无介入和非选择β受体阻滞剂治疗的患者;④患者和家属签署知情同意书。本研究已获得辽阳市中心医院伦理委员会批准。
1.1.3 排除标准
①严重的心肺肝肾脑等脏器功能不全者;②食管溃疡和食管恶性肿瘤疾病;③失血后生命体征不稳定者;④肝性脑病、意识障碍和其他精神心理疾病,无法配合内镜诊治者。
1.2 方法
1.2.1 物品准备
设备:胃镜(H260/HQJ260/HQ290/Q150,奥林巴斯,日本);支气管镜(P150,奥林巴斯,日本)。
器械:注射针(NM200-0423,奥林巴斯,日本,批号20181129);可旋转组织夹(和谐夹,南京微创医学科技,批号20191117)。
药品:医用胶(0.5 mL涂抹型;北京福爱乐科技发展有限公司,批号20190424);聚桂醇注射液(10 mL:100 mg;陕西天宇制药有限公司,批号20160103);注射用奥美拉唑(40 mg;英国阿斯利康,批号1602a01);硫酸依替米星(100 mL:0.1 g;江西制药有限公司,批号20180206)。
1.2.2 操作方法
术前准备及麻醉起效后,消毒铺单。组织胶注射治疗采用“三明治”夹心法[5]。硬化剂注射治疗根据静脉曲张的程度减少或增加剂量,一般不超过40 mL。食管胃底静脉曲张破裂出血时常伴随着胃黏膜和食管黏膜炎症水肿,容易发生细菌感染[1-2,6]。在本次研究中采用广谱抗生素依替米星进行抗感染治疗,对大部分G+及G-菌有良好抗菌作用。
A组患者在注射针内预先用50%葡萄糖注射液充满,内镜下选中靶静脉,保持注射针稳定后,出针,并迅速刺入靶静脉,快速注入1.0~2.0 mL组织胶,再注入1.3 mL 50%葡萄糖,组织胶推入后退出针芯,再将针鞘退离注射点,再注入5%葡萄糖液5 mL,冲洗注射针,预防注射针堵塞。
B组患者在注射针预先置入硬化剂,内镜下选中靶静脉,保持注射针稳定后,出针,并迅速刺入靶静脉后注入3~5 mL硬化剂,随后注入组织胶1.0~2.0 mL/点,之后步骤与上述A组步骤相同。
术后处理:术后6~8 h流质饮食,术后24 h后半流质饮食。术后静滴注奥美拉唑40 mg,2次/d;依替米星0.3 g,1次/d,共静滴3 d。
1.2.3 观察指标
采用内镜评估并记录A、B两组患者的早期排胶出血情况、组织胶的注射总量以及注射后异位栓塞发生情况。门诊随访1次/3~4周,周期为3个月。
1.3 统计学方法
采用SPSS 20.0统计学软件系统,计量资料用均数±标准差(x±s)表示,两组比较用t检验;计数资料用率(%)表示,两组比较用2检验。P值<0.05认为有统计学意义。
二、结果
2.1 基本资料
本研究192例患者全部获得随访。A、B两组性别、年龄、肝功能、凝血功能、门静脉直径及Child-Pugh评分比较,无显著性差异,P>0.05(表1)。
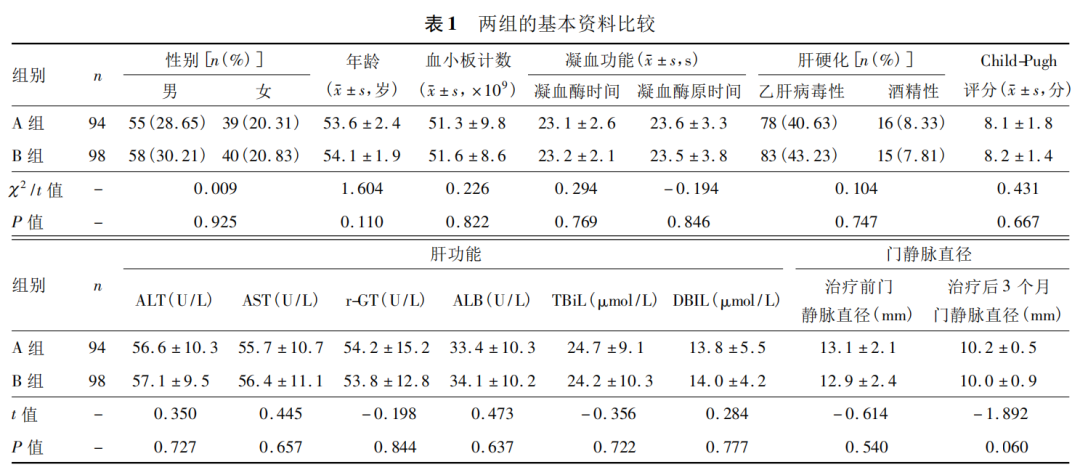
2.2 并发症情况
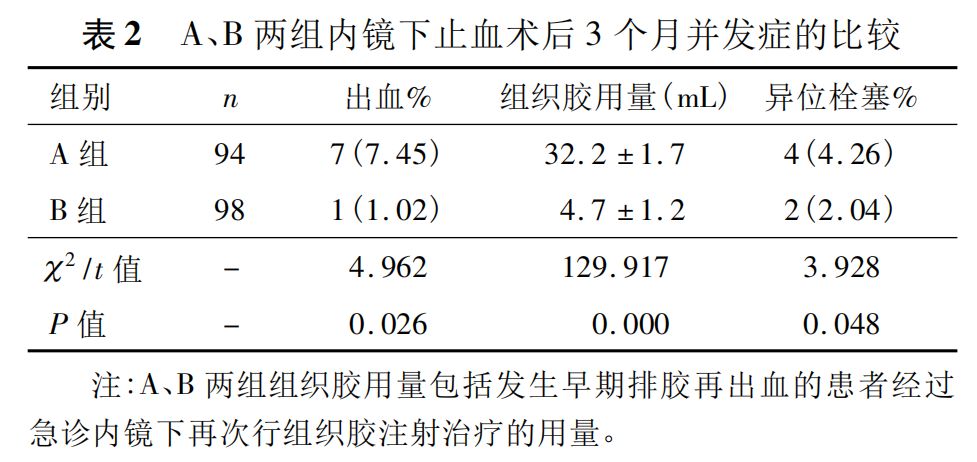
A组和B组内镜下止血术后3个月并发症的比较(表2)。A组早期排胶出血率、组织胶用量及异位栓塞发生率均明显高于B组,P<0.05,具有统计学意义(图1)。A组术后排胶出血率为7.45%明显高于B组的1.02%,P<0.05;A组组织胶用量为(32.2±1.7)ml明显高于B组的(4.7±1.2)mL,P<0.05;A组术后异位栓塞发生率为4.26%明显高于B组的2.04%,P<0.05。早期排胶再出血的患者经过急诊内镜下再次组织胶注射治疗、辅助止血药物治疗后,均获得有效止血,均无糜烂等其他并发症发生。
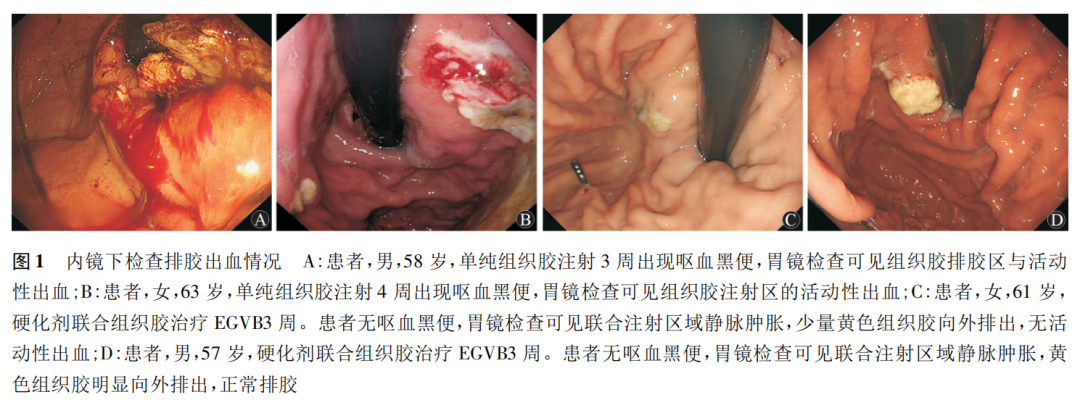
三、讨论
门静脉高压的并发症中,EGVB是最严重最凶险的。肝硬化患者因为门静脉压力增高发生EGVB的患者约占5%~15%,与肝功能损害的严重程度相关[1-2,7]。在肝硬化初次发生EGVB的患者中有15%~20%的死亡率,原因在于无法紧急有效的控制出血,发生再出血后的死亡率将更高[8],因此EGVB被誉为目前公认的门脉高压最为凶险的并发症之一[9-10]。有效的快速止血并做好止血后的预防再出血工作是临床医生的关注焦点。
内镜下止血、血管活性药物、三腔两囊管压迫等是目前紧急救治EGVB的主要治疗方法。由于内镜技术的快速发展,镜下止血技术快速、便捷、准确,大大降低了出血死亡率,已经成为预防和治疗EGVB的主要手段。内镜止血技术主要有:硬化剂注射术(EIS)、组织胶注射术(TAI)、套扎术、钳夹术等。内镜下EIS和TAI技术的学习曲线短,与其他内镜技术和外科干预手段相比更适合中心级医院的开展,快速、便捷、操作简单,更容易获得广泛的临床推广和应用[11]。
Soehendra教授在1986年首次报道了内镜下组织胶注射治疗胃底静脉曲张获得较好疗效[12-13]。但研究发现:单一方法治疗胃底食管静脉曲张不能够满足临床需要,组织胶作为一种异物从血管内排出的过程中,若血管未完全闭塞,容易造成早期排胶出血[14-16]。国内学者研究发现:胃底静脉曲张组织胶注射术后组织胶早期排出出血率高达19.7%[3],而国外相关报道甚少。研究还发现:内镜下联合治疗可更有效的止血,预防再次出血,且成功率高、并发症少[17-18]。本研究中A组和B组的基线资料无显著性差异,A组采用组织胶注射治疗共94例;B组采用硬化剂联合组织胶注射治疗共98例。A组术后排胶出血率为7.45%明显高于B组的1.02%,P<0.05;A组组织胶用量为(32.2±1.7)ml明显高于B组的(4.7±1.2)ml,P<0.05;A组术后异位栓塞发生率为4.26%明显高于B组的2.04%,P<0.05。回顾性分析结果表明:EGVB的内镜下EIS联合TAI治疗,可明显著降低早期排胶出血率、减少组织胶用量和异位栓塞的发生。单纯采用内镜下TAI较EIS联合TAI易发生早期排胶出血,因为组织胶注射后的血管发生系列的炎性反应、慢性肉芽肿异物反应和纤维化,纤维化的血管可使血管闭塞,而单纯组织胶注射的时间内血管未达到充分闭塞,即发生排胶出血。研究表明:肉芽肿向纤维化转变的过程发生在组织胶注射于血管后的3~4周,在此过程中组织胶将逐渐排出,如果此刻血管的肉芽肿向纤维化转变顺利完成,血管闭塞完毕,则组织胶可顺利排出;如果血管肉芽肿向纤维化转变延迟、血管闭塞延迟继而导致组织胶的排出时间相对提前,即可发生再出血。同时,单纯应用组织胶注射还存在异位栓塞、胸痛、发热等并发症的风险[19-20]。
因此,保证血管的肉芽肿向纤维化转变顺利完成,加速血管闭塞速度,有利于组织胶排出,减少排胶出血率、降低异位栓塞率。本研究发现:硬化剂可即刻破坏血管内皮细胞,血管纤维化加快,血栓形成引发血管闭塞。日本学者Maruyama通过影像学评估发现:内镜下EIS联合TAI治疗EGVB还有助于闭塞组织胶未彻底控制的曲张静脉[21]。而国内学者发现预先注射硬化剂再注射组织胶可加速血管纤维化速度利于组织胶排胶的顺利完成,减少排胶出血[22-23]。另外,在内镜下治疗伴有胃-肾、脾-肾分流道的静脉曲张时,内镜下TAI治疗会受到自发性分流道的影响,组织胶用量和异位栓塞率增加,静脉曲张伴有自发性分流道时更明显,栓塞风险明显增加[24]。因此要了解门脉高压侧支循环的解剖结构,熟悉其并发症对于诊治EGVB是必要的。本组98例患者采用内镜下EIS联合TAI治疗EGVB,该联合注射模式,安全性高,对于胃底静脉曲张合并自发性分流的患者也具有优势[25]。综上所述,EIS联合TAI可预防和降低并发症:原因在于硬化剂破坏血管内皮细胞、加速血管纤维化;血管内皮与硬化剂注射后的血管通道的摩擦力增加,阻碍硬化剂和后注入的组织胶的流动性,继而减少分流血管的异位栓塞。
并且,EIS联合TAI治疗能够降低相关医用耗材的损耗。Zeng等采用EIS联合TAI治疗EGVB发现:组织胶的注射用量明显减少[26]。比较本研究组织胶使用量发现:EIS联合TAI治疗方法的组织胶使用量明显减少,从而降低患者的医疗费用[27-28]。当然,采用内镜下EIS联合TAI治疗EGVB,必须严格掌握注射针的进针角度和深度:硬化剂注射时进针角度不得超过30°,进针不宜太深,减少误伤食管穿孔、出血的发生,准确的选取需要注射的靶静脉和注射点,严格把握注射的速度和量,拔针时应先缩针后拔针,否则容易引起食管穿孔或大出血[29]。术后,我们仍要关注患者的肝功能的康复情况,口服普萘洛尔或纳多洛尔降低门脉压力[30],加强患者的教育管理,提高依从性,规律随访,定期复查,使内镜下EIS联合TAI治疗EGVB在临床中更好的发挥有效作用。
本研究结果表明采用内镜下EIS联合TAI治疗EGVB,能够显著降低早期排胶出血率和异位栓塞率,临床疗效满意,值得推广应用,但对于不同出血风险程度的患者是否能够带来同样的获益尚不明确,需要进一步的临床研究。
参考文献






