发布时间:2025-01-14 13:43:27 来源: 浏览次数:847
《中国医学计算机成像杂志》2024 年第 30 卷 第 6 期
超声造影评估微波联合聚桂醇消融治疗子宫肌瘤疗效的临床研究
王 娜、郭学佳、陈江红、刘文聪(河北省石家庄市河北医科大学第一医院超声科,石家庄 050000)
摘要:目的:探究超声造影 (CEUS) 评估微波联合聚桂醇消融治疗子宫肌瘤患者的临床疗效。
方法:回顾性分析本院2023年4月—2023年11月收治的315例长径>5 cm的子宫肌瘤患者临床资料,所有患者均接受微波消融联合聚桂醇治疗,观察手术情况,于治疗前及治疗后3个月进行CEUS与增强MRI检查,分析不同增强强度、增强形态、充盈缺损状态子宫肌瘤患者术后消融率差异,对比治疗前后子宫肌瘤CEUS时间强度曲线参数变化,探讨CEUS与增强MRI对消融率评估结果的一致性。结果:术前造影低增强患者术后消融率高于等增强患者,等增强高于高增强患者,有充盈缺损、不均匀增强患者术后消融率高于无充盈缺损、均匀增强患者 (P<0.05)。CEUS时间强度曲线参数分析结果显示,相较于治疗前,子宫肌瘤微波消融联合聚桂醇治疗后达峰时间延长,峰值强度降低 (P<0.05)。治疗后 3 个月,CEUS 评估子宫肌瘤消融率包括 80%~100% 者 222 例,60%~80% 者 78 例,40%~60% 者 15 例,其中 296 例与增强 MRI 评估结果相符,符合率为93.97%;治疗后CEUS评估微波消融联合聚桂醇治疗长径>5 cm子宫肌瘤80%~100%、60%~80%、<60%消融率与增强MRI评估一致性的Kappa值分别为0.887、0.839、0.868。结论:CEUS和增强MRI检查在微波消融联合聚桂醇治疗长径>5 cm子宫肌瘤的术后疗效评估中,具有较高的一致性。关键词:子宫肌瘤;微波消融术;聚桂醇;临床疗效;超声造影
子宫肌瘤为女性常见良性生殖肿瘤,在育龄期女性中,发生率达20%~40%[1]。对于长径≤5 cm的子宫肌瘤,微波消融疗效显著,但若肌瘤较大,消融疗效不足。子宫肌瘤的体积与其滋养血管内径、血流速度呈现正相关,当肌瘤体积增大时,滋养血管内径随之增粗,同时血流也相对更加丰富 [2]。与此同时,为防止消融过程中的热损伤,治疗时往往会保留一定的安全距离,因此对于长径>5 cm 的肌瘤,完全消融的难度较大 [3]。硬化剂注射目前已成为子宫肌瘤治疗新手段,聚桂醇为常用硬化剂,聚桂醇注射可破坏血管内皮,使滋养血管腔内血液凝固,形成血栓,病灶结构组织失去营养,从而实现肌瘤灭活。超声造影(contrast?enhanced ultrasound,CEUS) 通过造影剂注射反映组织内部的血流灌注状态,不仅可有效显示血流灌注区,还可实时观察病灶灌注强度与和消退 [4]。本研究首先将聚桂醇注入子宫肌瘤周边滋养血管,之后进行微波消融。既往关于CEUS在子宫肌瘤高强度聚焦超声中的应用研究较多,但关于CEUS在微波消融联合聚桂醇治疗长径>5 cm 子宫肌瘤疗效评估价值相关研究较少 [5]。本研究通过与增强 MRI 对比,阐述CEUS在子宫肌瘤微波消融联合聚桂醇疗效评估中的应用价值,旨在为临床疾病治疗提供参考,报告如下。
方 法
1 研究对象
回顾性分析本院 2023 年 4 月—2023 年 11 月收治的315例长径>5 cm的子宫肌瘤,并接受微波消融联合聚桂醇治疗的患者临床资料。年龄23~49岁,平均(36.74±4.07) 岁。肌瘤分型:肌壁间191例,浆膜下124例;长径5.2~9.2 cm,平均 (6.83±0.39) cm。
2 纳入与排除标准
纳入标准:(1) 符合《中华妇产科学》子宫肌瘤诊断[6],结合临床症状、超声、盆腔MRI确诊,肌瘤最大径>5 cm;(2) 于本院接受微波消融联合聚桂醇治疗;(3) 年龄≥18岁,非绝经期,有性生活、具生育要求;(4)肌瘤数目<3个;(5)临床资料完整。
排除标准:(1) 合并其他非良性病变;(2) 合并盆腔、生殖道急性炎症;(3) 可疑肉瘤变;(4) 严重心、脑血管病史,如脑血管意外、心力衰竭者;(5)合并其他严重器质功能疾病;(6) 合并免疫、血液系统疾病;(7) 过度肥胖;(8) 盆腔粘连严重或腹部严重瘢痕;(9) 穿刺路径中,膀胱、直肠等遮挡,或位置超穿刺针到达上限。
3 方法
3.1 治疗方法
超声下腹部扫查,穿刺点确定,观察肌瘤信息及周围情况,造影观察瘤体血供。常规麻醉、消毒、铺巾,穿刺针置入肌瘤包膜,寻找滋养血管,往其起始周围包膜下,注射 10~20 mL 聚桂醇,聚桂醇扩散至瘤体周边,停止注射,待周边彩色血流信号消失,穿刺针拔出,之后进行人工腹水和微波消融。生理盐水注入,人工腹水,术野暴露,超声引导下,微波穿刺针植入,按先深后浅、由中间到两边实施消融。微波输出功率45~55 W,根据实际情况调整。术中观测消融区回声改变,注意避免损伤周围危险区。
3.2 超声造影检测
所有患者分别于治疗前、治疗后 3 个月进行CEUS 检 查 , 采 用 彩 色 多 普 勒 超 声 (飞 利 浦 ,EPIQ7),腹部电子凸阵探头,频率 3~8 MHz。使用SonoVue 造影剂 (意大利,Bracco),肘浅静脉注射(2.4 mL),随后,5 mL 生理盐水冲管,观察并记录肌瘤信息及血流灌注状态。
3.3 MRI检查所有患者分别于治疗前、治疗后3个月进行增强MRI检查,采用 MAGNETOM Vida 3.0 T 超导高场强MRI 扫描仪 (德国西门子),采集 T1WI、T2WI 平扫及 T1WI增强矢状位、横断位、冠状位图像,造影剂为钆喷酸葡甲胺,剂量 0.1 mmol/kg。观察并记录肌瘤信息及血流灌注状态。
4 效果评价由 2 名高年资影像学医师阅片,测定肌瘤体积(V):V=0.523 3×D1×D2×D3 (D1、D2、D3 分别为肌瘤长径、前后径、左右径);计算无灌注区体积消融率:消融率=无灌注区体积/靶肌瘤体积×100%。
5 统计学方法
采用 SPSS20.0软件分析。计数资料以 n (%) 表示,组间行 χ2检验比较;正态分布的计量资料以 xˉ ±s表示,组间行独立样本t检验比较,组内治疗前后行配对样本 t 检验比较。通过一致性检验分析 CEUS 与增强MRI结果一致性:Kappa≥0.75为一致性好;0.4~0.75 为一般;<0.4 为差,P<0.05 代表差异有统计学意义。
结 果
1 手术情况
所有患者均顺利完成微波消融联合聚桂醇治疗,治疗过程中未出现肠穿孔等严重并发症,共有 53 例患 者 术 中 或 术 后 出 现 不 良 反 应 表 现 , 发 生 率 为16.83% (53/315),包括术中轻中度腹痛 27 例,持续10~30 min,术后卧床自行缓解;术后 1~2 d 出现38.5℃以下低热者 10 例,持续 2~5 d 后恢复正常;术后恶心呕吐者16例,未经特殊处理自行缓解。
2 术前 CEUS 不同增强强度、增强形态、充盈缺损状态子宫肌瘤患者术后消融率比较
术前造影低增强患者术后消融率高于等增强患者,等增强患者术后消融率高于高增强患者,有充盈缺损、不均匀增强患者术后消融率高于无充盈缺损、均匀增强患者 (P<0.05)。见表1。
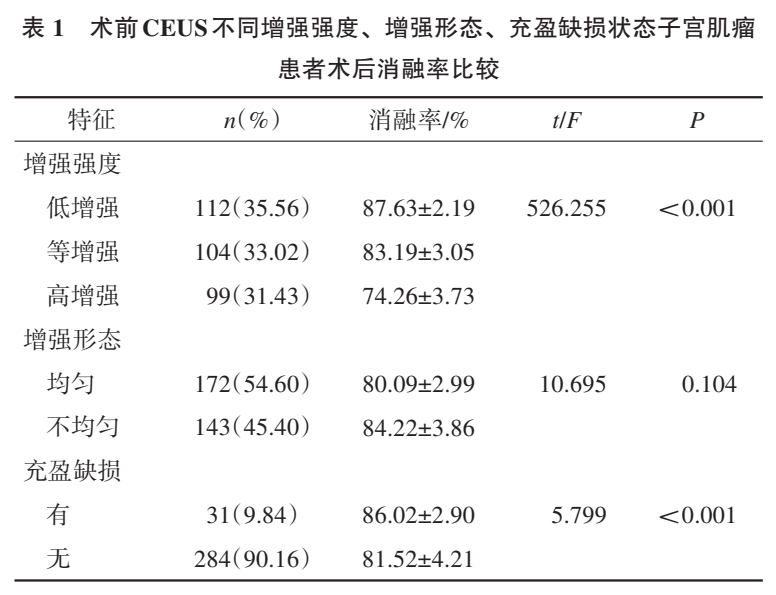
3治疗前后子宫肌瘤 CEUS 时间强度曲线参数比较
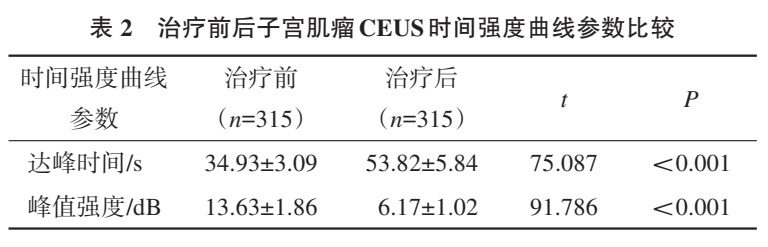
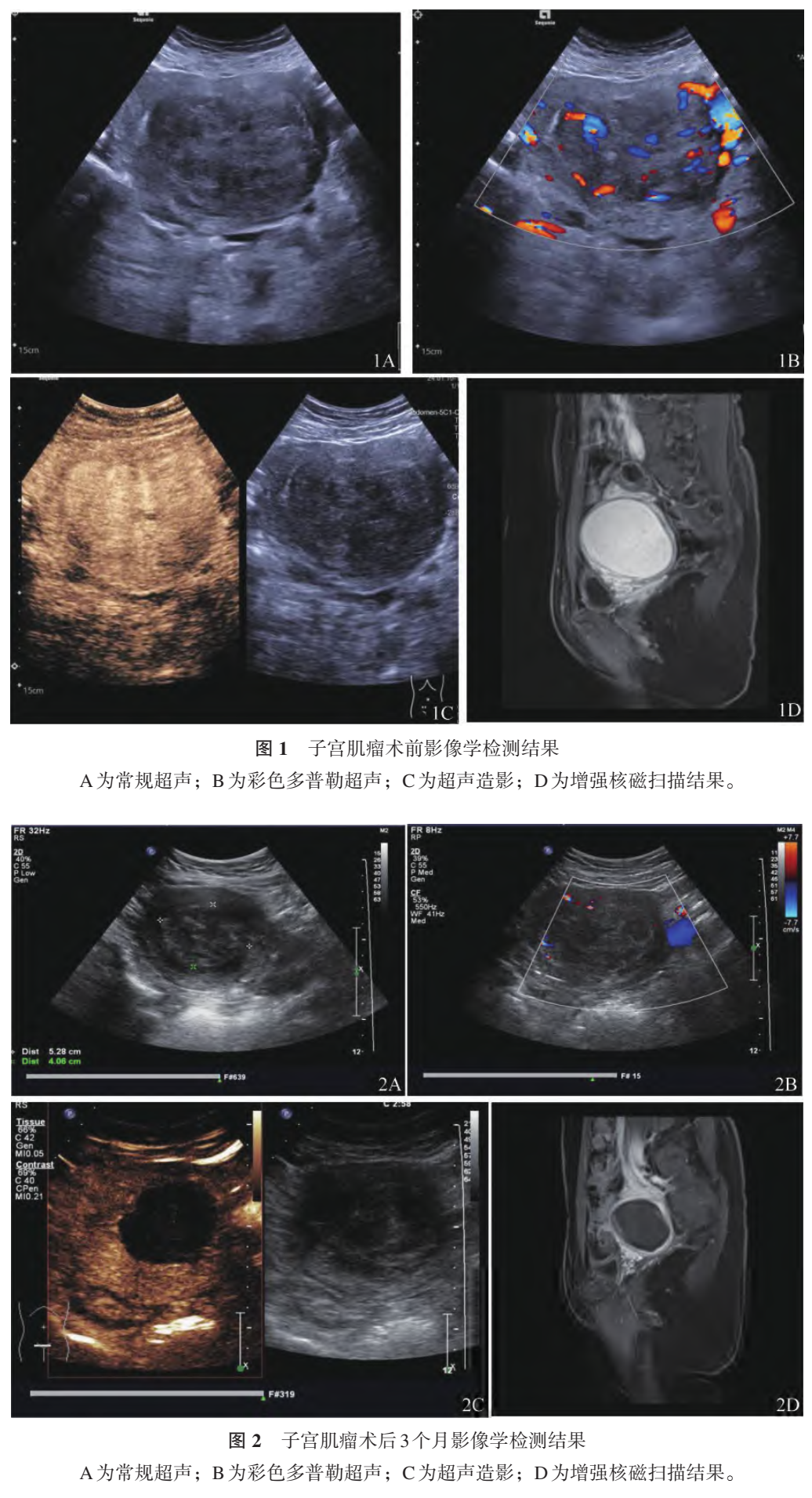
CEUS时间强度曲线参数分析结果显示,相较于治疗前,子宫肌瘤微波消融联合聚桂醇治疗后,残余瘤组织达峰时间延长,峰值强度降低 (P<0.05)。见表2、图1与图2。
4子宫肌瘤治疗后 CEUS 与增强 MRI 疗效评估结果对比
治疗后,CEUS 评估消融率包括 80%~100% 者222例,60%~80%者 78例,40%~60%者 15例,其中296 例与增强 MRI 评估结果相符,符合率为 93.97%。见表3。

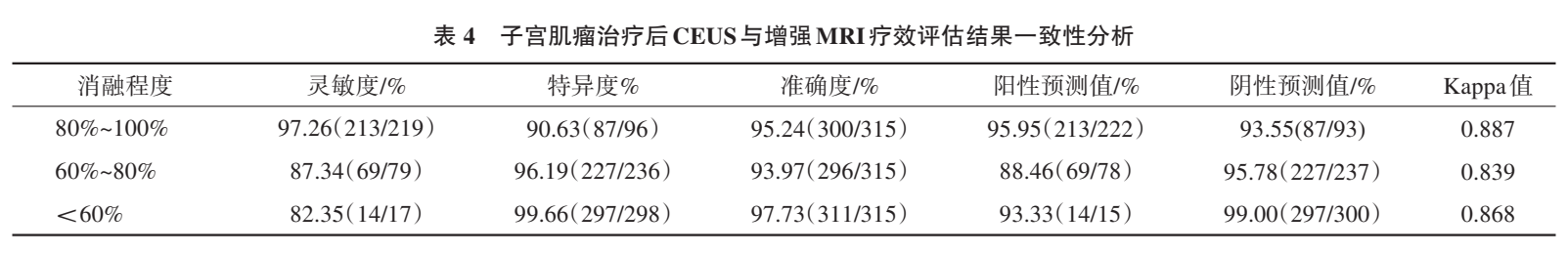
5子宫肌瘤治疗后 CEUS 与增强 MRI 疗效评估结果一致性分析
治疗后,CEUS评估微波消融联合聚桂醇治疗长径>5 cm 子宫肌瘤 80%~100%、60%~80%、<60%消融率与增强 MRI 评估一致性的 Kappa 值分别为0.887、0.839、0.868。见表4。
讨 论
子宫肌瘤可引起患者盆腔压迫症状、子宫异常出血、疼痛、不孕等,据相关数据统计显示,子宫肌瘤患者中约有 20%~30% 具有不孕症状 [7]。聚桂醇注射可对滋养血管造成破坏,防止肌瘤细胞增殖;再加上微波热消融,进一步使肌瘤细胞坏死,二者联合可达到双重治疗目的。既往戚云峰等 [8]的研究显示,对于长径>5 cm 的子宫肌瘤,微波消融联合聚桂醇治疗具有创伤小、恢复快等特点,能有效弥补单一微波消融不足,提高肌瘤的缩小率。
微波消融联合聚桂醇治疗长径>5 cm 子宫肌瘤的疗效评价需基于临床评价和影像学评价的基础之上,术后随访中观察病灶消融情况、症状改善情况,术后影像学评价确定肌瘤消融情况尤为重要。目前,超声为临床子宫肌瘤诊断常用方法,可反复操作,可观察到肌瘤大小、位置、血流变化等诸多信息,对肌瘤消融情况作出初步判断,但对新生血管、微血管、坏死范围等的评估存在一定的不足,不能反映肌瘤坏死程度及残存情况 [9]。MRI可有效反映子宫肌瘤手术前后大小、信号、血供变化,是术后疗效的有效评估手段,但其成像速度较慢,禁忌证较多,应用受到一定的限制 [10]。近年来,随着 CEUS 技术飞速发展,其也逐步被应用于子宫肌瘤诊断与治疗中。CEUS检查反映病灶血液灌注,根据子宫肌瘤治疗前后影像学变化,可实现瘤体的立体观察与测量,反映肿瘤血管分布状态,以此判断靶区组织坏死程度。Cheng等 [11]的研究表明,子宫肌瘤高强度聚焦超声治疗后,病灶出现凝固性坏死,CEUS可依照组织血流灌注状态勾勒出病灶坏死范围,且与病理结果相关性良好。范宏杰等 [12]的研究也显示,CEUS 检测简便易行,消融区内部造影无增强,而未消融组织呈现强化状态,二者对比明显,可以此判断消融范围。
子宫肌瘤血流状态是子宫肌瘤消融治疗疗效的重要影响因素,肌瘤血供丰富则其血液循环迅速,治疗过程中微波消融能量易随血液流逝,使得治疗温度达不到肌瘤凝固性坏死的阈值温度,从而使得消融体积减少,疗效变差。子宫肌瘤CEUS增强强度与血供状态关系密切,强化越明显代表血供越丰富。本研究显示,子宫肌瘤术前CEUS结果显示增强强度越高,疗效越差。CEUS不均匀增强、充盈缺损提示肌瘤变性坏死,肌瘤坏死区域超声能量易沉积,可拥有较佳的消融疗效。本研究中术前CEUS不均匀增强、充盈缺损状态子宫肌瘤患者微波消融联合聚桂醇治疗后消融率高于均匀增强、无充盈缺损子宫肌瘤患者,CEUS均匀增强提示子宫肌瘤的平滑肌细胞、结缔组织有序排列,血流灌注佳,疗效较差 [13]。CEUS时间强度曲线可定量分析组织器官中造影剂的分布和动态改变,为子宫肌瘤的疗效评估提供动态量化参考指标。达峰时间反映了组织血流灌注速度,峰值强度则与感应区平均血流量呈正比。Wang等 [14]的研究发现,高强度聚焦超声治疗后CEUS可清晰显示子宫肌瘤无灌注区域范围,CEUS时间强度曲线幅度下降,治疗前后血流灌注具有显著性差异。本研究发现,子宫肌瘤微波消融联合聚桂醇治疗后,坏死区无造影剂灌注,而残余瘤组织仍有造影剂灌注,治疗后时间强度曲线最高点低于治疗前,达峰时间延迟、峰值强度降低,表明肌瘤血流灌注减慢,血容量减少,微波消融联合聚桂醇治疗有效。
王英姿等 [15]的研究显示,CEUS 检查可清楚显示子宫肌瘤及非灌注区情况,与增强 MRI 检查结果高度一致,可为 HIFU 治疗子宫肌瘤疗效评估及临床治疗方案的制定提供可靠依据。但临床关于CEUS在微波消融联合聚桂醇治疗疗效价值评估中,相关研究较少。本研究显示,接受微波消融联合聚桂醇治疗的315 例长径>5 cm 子宫肌瘤患者 CEUS 造影消融率显示结果中,有222例与增强MRI检查结果相符,符合率为93.97%,治疗后CEUS评估微波消融联合聚桂醇治疗长径>5 cm 子宫肌瘤 80%~100%、60%~80%、<60%消融率与增强MRI评估一致性Kappa值分别为0.887、0.839、0.868,一致性均较佳。上述研究结果表明,CEUS可直观观察微波消融联合聚桂醇治疗长径>5 cm 子宫肌瘤消融范围、消融程度,评价临床疗效,CEUS是増强MRI检查的补充或替代手段,其临床适用性高,其造影剂具有较高的安全性,过敏反应风险低,且造影剂主要经肾、肺泡代谢,进而排出体外,即使是对于存在甲状腺疾病、慢性肾功能不全、带金属节育器女性患者,均可使用。
综上所述,CEUS和增强MRI检查在微波消融联合聚桂醇治疗长径>5 cm 子宫肌瘤术后疗效评估中具有较高的一致性。

