中国超声医学杂志2016年11月第32卷第11期
超声引导下聚桂醇辅助射频消融术治疗子宫肌瘤的临床价值
戚云峰、董晓秋、张立维、王思明、邵小慧
(150001哈尔滨市,哈尔滨医科大学附属第四医院超声科)
摘要:
目的:探讨超声引导自凝刀射频消融(RFA)联合聚桂醇硬化治疗子宫肌瘤的疗效。
方法:超声引导下自凝刀RFA症状性子宫肌瘤患者102例,共114个肌瘤。治疗后3个月复查病灶,排除无血流及造影剂灌注的病例,将剩余22个子宫肌瘤随机平均分成两组,分别行超声引导下RFA补充治疗及聚桂醇硬化治疗。
结果:初次RFA后3个月与治疗前相比,114个子宫肌瘤血流分级明显下降(P<0.05)。需补充治疗的22个子宫肌瘤中,浆膜下肌瘤近浆膜侧周边、内部及近黏膜侧内部血流量明显多于肌壁间与黏膜下肌瘤。补充消融组完全消融率63.6%(7/11),硬化治疗组完全硬化率100%(11/11),两组相比,差异有统计学意义(P<0.05)。
结论:超声引导聚桂醇硬化辅助自凝刀RFA子宫肌瘤,较单一RFA更为安全。针对近浆膜侧血流丰富的浆膜下肌瘤,采取聚桂醇硬化作为补充治疗在临床上实用价值更大。
关键词:
超声引导,射频消融,硬化治疗,子宫肌瘤
子宫肌瘤是育龄女性最常见的盆腔肿瘤,部分患者伴有临床症状,包括月经过多、盆腔疼痛、压迫症状、内分泌紊乱及不孕等[1],需积极治疗。近年,射频消融(radio frequency ablation,RFA)治疗肌瘤逐步推广应用,但对位置不佳及体积较大的肌瘤存在治疗不彻底的问题,经阴超声引导聚桂醇硬化治疗精准靶向[2],可弥补RFA的不足,本研究旨在评价超声引导RFA联合聚桂醇硬化治疗子宫肌瘤的临床疗效和安全性。
一、 资料与方法
1.1 研究对象
2013年1月-2016年3月来我院自愿接受治疗的有症状肌瘤患者102例,共114个肌瘤,肌壁间68个,半浆膜下26个(外凸浆膜部分<1/2),黏膜下20个(无蒂)。年龄29~44岁,平均(38.5±3.2)岁,肌瘤1.9~4.8cm,平均(3.0±0.9)cm。均无生殖系统急性炎症、癌前病变、恶性肿瘤及其他严重的内科疾病。
1.2 仪器与方法
(1)仪器 采用Logiq E9 c1-5凸阵及Ric5-9-D阴式容积探头和BBT-RF-E妇科多功能射频治疗仪;造影剂为SonoVuE(Bracco公司),硬化剂为聚桂醇注射液。
(2)方法 ①术前准备:经阴及经腹超声、血常规、凝血功能、血糖等常规检查,签署治疗知情同意书。②血流分级标准[3]:按Adler半定量法分为4级,0级:未见血流信号;Ⅰ级:可见1~2处点、棒状血流信号;Ⅱ级:可见3~4处点状血流信号或一条长度超过或接近瘤体半径的血管;Ⅲ级:可见4条以上血管,粗细不等,交织成网。③经腹超声引导自凝刀射频消融:适度充盈膀胱取截石位,经腹超声监视下将自凝刀经宫腔缓慢插入肌瘤的中心或稍偏向一侧,消融温度达到标准后,射频治疗仪会自动停止工作,同样方法消融其他部位。④经阴超声引导聚桂醇硬化治疗:排空膀胱取截石位,避开重要器官及血管,采用18G PTC针经阴道穿刺至肌瘤造影剂灌注区,转动穿刺针多方向注入聚桂醇。
1.3 统计学方法
采用SPSS 19.0软件包进行统计处理,计数资料采用χ?检验或Fisher确切概率法统计,P<0.05为差异有统计学意义。
二、 结果
2.1 初次RFA治疗前及治疗后3个月子宫肌瘤血流分级
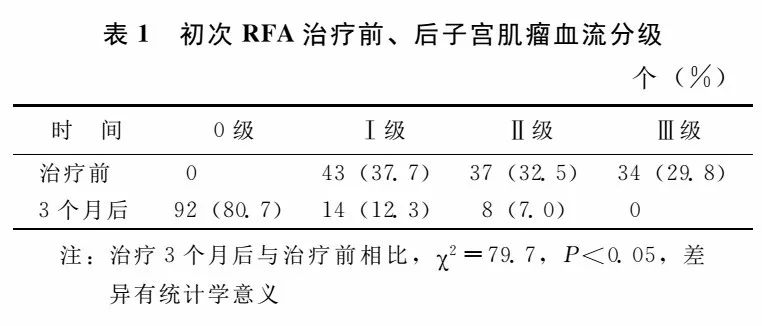
初次RFA前血流分级:Ⅰ级占37.7%(43/114),Ⅱ级占32.5%(37/114),Ⅲ级占29.8%(34/114);RFA后3个月:0级占80.7%(92/114),Ⅰ级占12.3%(14/114),Ⅱ级占7.0%(8/114),与治疗前相比,差异有统计学意义(P<0.05)(表1)。
2.2 待补充治疗子宫肌瘤血流分布
初次RFA后3个月复查超声造影(contrast-Enhanced-ultrasound,CEUS),22个有造影剂灌注的子宫肌瘤周边及内部共有灌注点42处,其中,浆膜下肌瘤近浆膜侧周边灌注点占38.1%(16/42),近浆膜侧内部灌注点占26.2%(11/42),近黏膜侧内部灌注点占16.7%(7/42),均明显多于肌壁间及黏膜下肌瘤(表2)。

2.3 补充治疗后CEUS结果
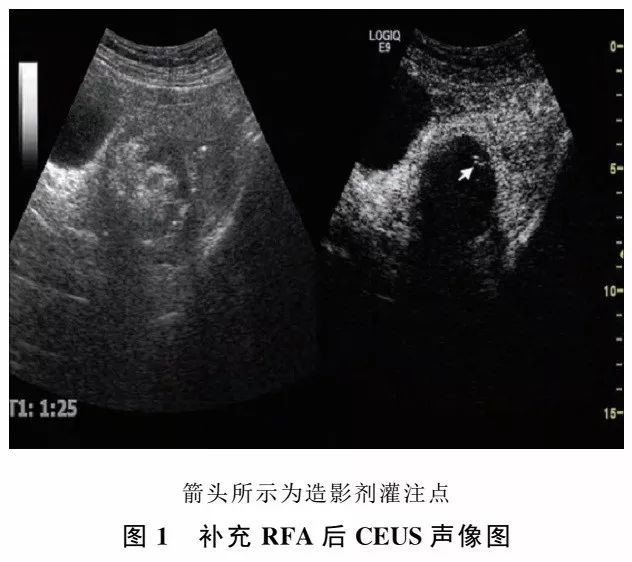
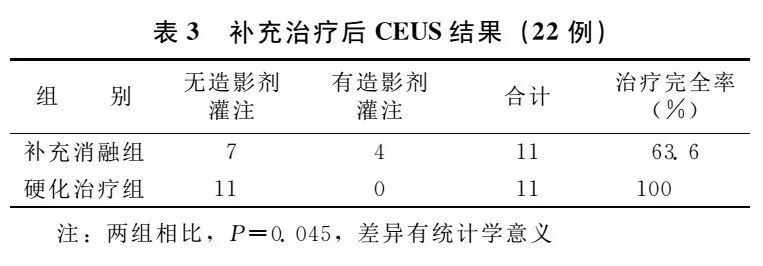
补充治疗后行CEUS,补充消融组完全消融率63.6%(7/11),其中4个浆膜下肌瘤近浆膜侧周边分别可见1处造影剂灌注点(图1);硬化治疗组未见造影剂灌注,完全硬化率100%(11/11),与补充消融组相比,差异有统计学意义(P<0.05)(表3)。
三、 讨论
子宫肌瘤是育龄女性最常见的良性肿瘤,常导致相应临床症状而影响患者生活质量。超声引导的RFA及硬化治疗通过使肌瘤去血管化而达到治疗目的,与传统手术相比有其独特优点[4],门诊就可操作,治疗后患者短期内即可正常工作。
本研究选取单个或两个肌瘤患者102例,114个肌瘤,初次RFA后与治疗前相比血流分级明显下降,初次RFA疗效显著。RFA后肌瘤因热损伤发生变性、坏死、血管闭塞等改变,同时启动修复机制,由于热损毁及肌瘤残存组织修复机制的共同作用,此时肌瘤血供主要来源于血管母细胞形成新的血管及残存成熟血管内皮细胞增殖和游走形成的小血管。
初次RFA后3个月复查CEUS,仍有22个肌瘤可见造影剂灌注区,浆膜下肌瘤占72.7%(16/22),其血流分布点主要位于近浆膜侧周边、内部及近黏膜侧内部,明显多于肌壁间及黏膜下肌瘤。因RFA过程中,为避免子宫穿孔及邻近器官热损伤,必须确保针尖与子宫浆膜间距尽可能大于安全距离,常致肌瘤浆膜侧消融不全。待补充治疗的4个肌壁间及2个黏膜下肌瘤均>3cm,较大肌瘤RFA后复发率高,因较大肌瘤需多次布针,由消融产生的气化现象会影响其周围组织显像,致使超声定位更加困难。
初次RFA后3个月,将出现再生或新生血管的22个肌瘤随机平均分成两组,分别治疗后CEUS检查,硬化治疗组治疗率(100%)明显高于补充消融组(63.6%)。RFA是应用射频能量产热使肌瘤组织凝固坏死,为避免子宫穿孔及邻近器官热损伤,常出现近浆膜侧肌瘤组织消融不全,补充消融组治疗后复查CEUS,有4个浆膜下肌瘤消融不全,造影剂灌注点均位于肌瘤浆膜侧周边处;而聚桂醇硬化治疗机制是破坏内皮细胞、促进血栓形成[5]、致管腔闭锁而达到治疗目的,可有效避免射频消融中邻近器官热损伤,对于近浆膜侧血运丰富的浆膜下肌瘤而言,相比RFA更为安全。另外,对消融不全的肌瘤,不选择射频消融后即刻聚桂醇硬化补充治疗,是因消融刀较粗,治疗后产生的治疗针道与宫腔相通,注入聚桂醇易从针道流出,降低硬化疗效,3个月后针道闭合良好时再次治疗更理想。
四、结论
对RFA不全及消融后出现新生血管的子宫肌瘤,行聚桂醇硬化补充治疗疗效显著;超声引导聚桂醇硬化辅助自凝刀RFA治疗子宫肌瘤,较单一RFA更为安全。针对近浆膜侧血流丰富的浆膜下子宫肌瘤,建议采取聚桂醇硬化作为补充治疗法在临床上实用价值更大。





