DOI:10.3877/cma.j.issn.2095-7157.2023.01.010
基金项目:国家重点研发计划(2022YFC2503604)
作者单位:100853 北京,解放军总医院第一医学中心消化内科医学部
通信作者:令狐恩强,Email:linghuenqiang@vip.sina.com;柴宁莉,Email:chainingli@vip.163.com
【摘要】目的 应用浓度为3%的聚桂醇溶液对建立的动物囊性肿瘤模型进行消融治疗,以评估其消融的安全性和有效性并探索该模型模拟胰腺囊性肿瘤的实用性。方法 自体移植法在30只雌性性成熟SD大鼠腹腔内建立子宫内膜异位囊肿模型,饲养4周后成功建模的囊肿随机分为两组分别注射3%聚桂醇溶液或生理盐水,饲养4周后打开腹腔观察囊肿消融情况,取标本进行病理学检查。结果 最终共收集了34个囊肿,形态学方面生理盐水组囊肿术前、术后均保持半球型,而3%聚桂醇溶液组囊肿术前的半球型消融后呈扁平瘢痕状;病理学方面生理盐水组标本上皮层单层柱状上皮细胞几乎无脱落,而3%聚桂醇溶液组标本上皮层单层柱状上皮细胞全部脱落,两组标本固有层均完整。消融术后囊肿无穿孔、腹腔脏器无损伤、大鼠无死亡。统计学分析两组消融有效率表明3%聚桂醇溶液具有良好的消融疗效。结论 3%聚桂醇溶液消融大鼠子宫异位囊肿模型安全且有效,初步表明3%聚桂醇可用于EUS-LA临床治疗。该模型一定程度上可以模拟胰腺囊性肿瘤。
【关键词】聚桂醇;囊性肿瘤;消融术;动物模型
聚桂醇注射液,主要成分为聚桂醇,化学名为聚氧乙烯月桂醇醚,作为一种硬化剂常用于内镜下食管胃底静脉曲张的治疗[1],在其他囊性病变例如消化道囊肿、肝囊肿、肾囊肿、甲状腺囊肿、卵巢囊肿等也有良好的治疗效果[2-6]。令狐恩强教授在2015年将聚桂醇率先应用于胰腺囊性肿瘤(pancreatic cystic neoplasm, PCN)上,我们的前期研究结果表明超声内镜引导下聚桂醇消融术(endoscopic ultrasound guided lauromacrogol ablation, EUS-LA)有良好的有效性及安全性。随访时间>1年的患者中,有51.4%的患者达到完全缓解,25.7%的患者达到部分缓解,并发症率仅为3.6%[7-13]。尽管二次消融可以进一步提高疗效,但是部分患者首次消融效果仍不够理想,多次消融将增加患者的经济负担。目前国内外临床应用的聚桂醇浓度为1%(10 ml∶100 mg,陕西天宇制药有限公司),尚无研究证实将聚桂醇的浓度提升到1%以上是否可以在安全的前提下进一步提高EUS-LA的疗效。
本研究旨在建立动物囊性肿瘤模型后应用浓度为3%的聚桂醇溶液对囊性肿瘤模型进行消融治疗,评估其安全性和有效性,探索该模型模拟PCN的实用性。
资料与方法
一、一般资料
选取10周龄雌性SD大鼠30只,体重约200~250 g,清洁环境饲养,温度20~25℃,相对湿度60%,每日光照明暗各12 h。饲养笼及饮用水采用高压灭菌法消毒,饲料和垫料采用辐照处理,垫料每日更换1次,不限制饮食。所有大鼠适应性饲养1周。试剂:3%聚桂醇溶液(10 ml∶300 mg,陕西天宇制药有限公司)、生理盐水、异氟烷、HE染色试剂盒。
二、实验动物和药物
采用自体移植方法建立大鼠子宫内膜异位囊肿模型。大鼠耳标编号1-30,经异氟烷气体麻醉后,仰卧位固定于手术板上,备皮后碘伏消毒腹部皮肤。在下腹中部耻骨联合上方1~2 cm处做一长约3 cm的纵向切口。腹部探查找到大鼠子宫,游离并结扎一侧子宫,切除卵巢,分离并切除一段约1 cm长的子宫。将子宫周边的脂肪组织在生理盐水中分离,然后将子宫切成0.5 cm×0.5 cm的2片。子宫内膜面朝向腹壁,用7-0缝线将子宫内膜固定在腹壁两侧血管丰富处。用青霉素钠溶液冲洗腹腔,逐层关腹。大鼠在标准条件下饲养4周,大鼠继续在清洁环境饲养4周。大鼠死亡的判定标准为停止活动或者对轻微刺激无反应,死亡的大鼠通过探查腹腔尸检以明确死因后退出实验。成功建模的标准为移植物区内有液体的红色囊状囊肿、囊肿表面覆盖结缔组织和毛细血管。造模失败的囊肿退出实验。
三、消融流程和评估
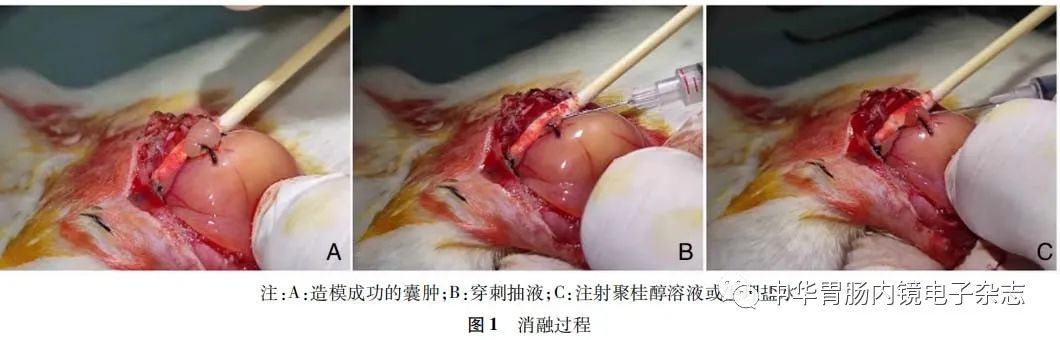
采用SPSS 25.0软件生成随机数表,将建模成功的囊肿依次标记,例如“1左”、“2右”,随后随机分为以下2组:A组为生理盐水组;B组为3%聚桂醇溶液组。打开大鼠腹部找到囊肿进行消融。注射器穿刺囊肿,抽出囊液后根据分组注射生理盐水或3%聚桂醇溶液。注射量为抽取的囊肿液量的80%,以保持囊肿轻微隆起。注射结束后拔针,棉签轻微压迫穿刺点,防止液体流出(图1)。腹腔用青霉素钠溶液冲洗,逐层关腹,腹部表面用碘伏消毒,在清洁环境继续饲养4周。
二氧化碳麻醉法处死大鼠,沿原切口打开腹腔,观察囊肿形态及对周围脏器的损伤程度。未消融的囊肿完整收集,已消融的囊肿收集残余瘢痕组织。瘢痕黏连严重无法收集的囊肿退出实验。标本用10%福尔马林溶液固定,H & E染色后,用低倍镜和高倍镜观察上皮层上皮细胞平均脱落率作为有效率,以固有层的完整性作为安全性评价标准。
四、统计学方法
由2名不参与手术的研究者分别记录实验数据和统计学分析。采用SPSS 25.0进行数据录入和分析。计量消融有效率,服从正态分布采用平均数±标准差(x±s)表示,不服从正态分布者采用中位数(四分位间距)表示。本实验是一个2组独立的样本实验,由2组实验数据组成。由于各组总体分布未知,且样本量较小,故采用多独立样本的非参数检验方法Mann-Whitney U检验。P<0.05为差异有统计学意义。
结 果
本研究30只大鼠中,2只大鼠造模手术过程中因麻醉剂过量死亡、4只大鼠造模术后4周内因囊肿造模失败导致缺血坏死、腹腔感染死亡,无大鼠在消融术后死亡。共有24只大鼠存活,存活率为80%;共36个囊肿成功建模,成功率为75%,2个囊肿因消融后黏连过度而不能完全收集而退出实验,因此,本研究最终共收集了34个囊肿。
一、形态学分析
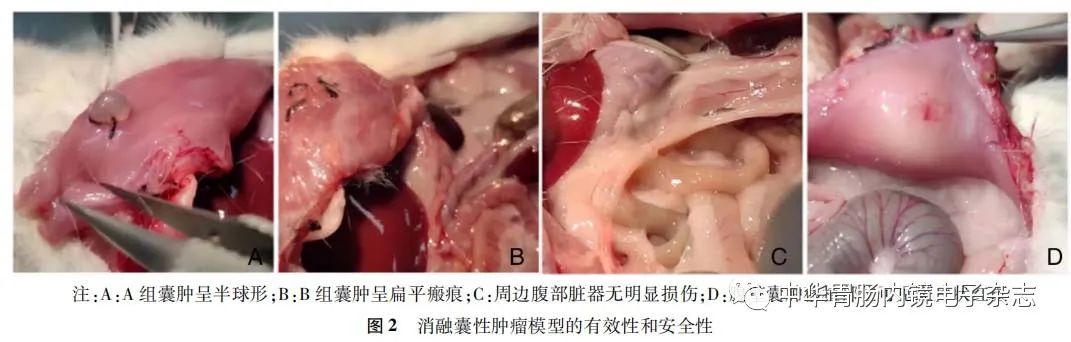
消融前囊肿模型呈半球形,含有透明或浑浊的液体,表面可见微血管。A组囊肿注射生理盐水后仍维持半球形囊性结构;B组囊肿注射对应浓度的聚桂醇溶液后被消融而失去囊性结构,形成扁平瘢痕(表1),个别大鼠囊肿移植部位可见斑片状红斑(图2)。
二、病理学分析
本研究共36个囊肿成功建模, 2个囊肿因消融后黏连过度而不能完全收集而退出实验。因此,最终共收集了34个囊肿。其中,A组16个、B组18个。低倍镜下观察各组标本由内到外依次为上皮层、固有层和肌层。各组固有层、肌层完整,大血管内充血、瘀血。B组标本由于炎症反应,固有层和肌层之间的界限模糊。高倍镜下观察各组标本上皮层单层柱状上皮细胞脱落情况,A组标本上皮层单层柱状上皮细胞几乎无脱落(图3),而B组标本上皮层单层柱状上皮细胞全部脱落(图4)。
A组16个囊肿标本消融有效率中位数62%,B组18个囊肿标本消融有效率中位数100%。采用非参数Mann-Whitney U检验评价消融有效率,检验结果显示A组与B组消融率差异有统计学意义(P<0.05,表2)。

讨 论
聚桂醇由亲水的十二烷基头和疏水的聚氧乙烯氧化链组成。其作用机制是改变药物接触表面的能量分数,降低表面张力,在细胞膜表面沉淀蛋白质,引起细胞膜破裂和细胞裂解,从而产生无菌性炎症和纤维组织增殖,达到硬化治疗的目的[14]。
本研究共收集标本34个。A组作为空白对照组,注射生理盐水后囊肿保持半球形结构,形态与注射前无明显变化;B组用3%聚桂醇溶液消融后,所有囊肿均失去术前的半球形结构变为扁平瘢痕。尽管部分囊肿瘢痕很难从腹壁分离,无法收集进行病理分析,但研究中无囊肿穿孔或完全溶解。手术探查发现消融后周边脏器未见明显损伤,部分大鼠腹壁的囊肿移植部位可见片状红斑,考虑药物的炎症反应。A组与B组标本的上皮层单层柱状上皮细胞脱落率经统计学分析显示,3%聚桂醇溶液与生理盐水相比具有显著的消融效果,初步表明3%聚桂醇溶液消融有效且安全。
聚桂醇溶液的消融作用已在不同的动物模型中得到证实。本课题组此前曾通过结扎鸭肠模拟PCN研究热消融的疗效和安全性,但由于上皮细胞的自发溶解导致实验结果无明显差异,最终实验终止。也有研究报道使用结扎的猪肠模拟胰腺导管内乳头状黏液腺瘤(intraductal papillary mucinous neoplasm, IPMN)来研究热消融的有效性和安全性[15]。该研究尽管设置了对照组以排除自发组织溶解的影响,但仍需要对结扎的动物小肠模拟囊肿进行体外热消融,并不适合模拟聚桂醇溶液在体内消融,有学者利用转基因小鼠建立胰腺黏液病变模型[16-19],虽然这些小鼠模型是理想的研究对象,但它们在技术上要求过高,难以广泛应用。
鉴于上述模型的不足,本研究决定采用大鼠子宫内膜异位囊肿模型,该模型已被一些学者用于验证聚桂醇的有效性和安全性。国内的一项研究表明,在大鼠子宫内膜异位模型中,1%聚桂醇注射液与0.5%聚桂醇溶液或空白对照相比,可使子宫内膜囊肿明显消融[20]。另一项研究表明,如果聚桂醇浓度保持在0.25% (<1%)以上,且不从囊肿模型中抽出,则有助于增强硬化治疗效果[21]。两项研究中聚桂醇的浓度都不超过1%,本研究团队首次使用浓度为3%的聚桂醇溶液进行研究。
本研究选择消融大鼠子宫内膜异位囊肿模型来研究PCN消融治疗基于两者之间相似的病因学、组织结构特点与消融流程。尽管一些病例与von Hippel-Lindau (VHL)基因的种系改变有关,浆液性囊腺瘤(serous cystic neoplasm, SCN)的致病性和病因学因素仍然很大程度上未知性。高达90%的VHL综合征患者发展为浆液性囊腺瘤。有研究提出VHL/HIF通路异常调控的中心腺泡起源,类似于其他富糖原肿瘤的起源。
胰腺黏液性囊腺瘤(mucinous cystic neoplasm, MCN)与肝胆、卵巢和其他器官的MCN有许多相同的临床病理特征。可以设想,在胰腺和其他器官的胚胎发生过程中合并的异位卵巢间质可能在激素失衡的环境下被激活,释放激素和生长因子,导致附近的导管上皮增生并形成囊性肿瘤,但是这个假设只能解释女性的MCN;另一种可能是卵巢型间质表现为持续性胎儿导管周间质,它可能对激素刺激产生反应并在激素刺激下增殖。
胰腺SCN和MCN的上皮是单层的立方或扁平细胞,细胞质清晰,胞浆边界清晰。核小而圆,染色质致密而均匀,核仁不明显。此外,囊肿含有透明的浆液或粘液液体。大鼠子宫内膜异位囊肿由内到外可分为上皮、固有层、肌层和浆膜。上皮为单层矩形柱状上皮,囊腔含有黏稠的透明或血色液体。造模成功后,子宫内膜在大鼠体内继续生长,并从扁平状的内膜逐渐形成囊肿样结构。注射聚桂醇溶液后,囊肿在体内逐渐发生消融,由囊状结构逐渐变为扁平瘢痕,而并未完全溶解。虽然大鼠子宫内膜异位症囊肿与PCN在胚胎学上没有明显的相似性,但它们的上皮细胞形态、结构层层次以及治疗和消融机制都有相似之处。因此,我们采用大鼠子宫内膜异位囊肿模型研究不同浓度聚桂醇溶液在胰腺囊性肿瘤消融中的有效性和安全性。
然而,使用聚桂醇溶液消融大鼠子宫内膜异位囊肿模型以模拟消融PCN仍然具有局限性;首先,子宫内膜的胚胎起源不同于胰腺囊性肿瘤。第二,子宫内膜上皮细胞随月经周期自发脱落,而胰腺囊性肿瘤上皮细胞不随月经周期自发脱落。我们设置了空白对照组以减少偏差。但由于样本量小,且部分B组囊肿消融后变为瘢痕组织,个别标本难以清晰显示各层病理结构。根据聚桂醇的药物作用机制,我们考虑这可能与炎症和纤维组织增生有关。
使用大鼠子宫异位囊肿模型研究不同浓度聚桂醇溶液对PCN的消融效果也有相应的优势。异位子宫囊肿与PCN在上皮细胞形态、囊肿生长方式、消融过程等方面有相似之处。消融后囊肿的形态初步提示3%聚桂醇溶液的有效且安全。然而,这种囊肿模型消融后部分瘢痕组织难以收集,从而一定程度上影响病理分析的结果。为了更好地探索不同浓度聚桂醇溶液用于消融的有效性和安全性,需要进一步改进才能成功收集更多子宫内膜异位囊肿标本。这些改进包括增加样本量,使用标本固定板,调整切片角度,以及增加标本的切片数量以计算平均值。
使用浓度为3%聚桂醇溶液消融大鼠子宫异位囊肿模型安全且有效,初步表明3%聚桂醇可用于EUS-LA临床治疗。该动物模型一定程度上可以模拟PCN,探索建立更适合的PCN模型有助于EUS-LA的进一步研究。
利益冲突:所有作者声明不存在利益冲突
作者贡献声明:高飞、李惠凯:设计实验、实施研究、撰写论文;冯秀雪:设计实验;杜晨:采集数据;韩珂:统计分析;柴宁莉教授:论文修改;令狐恩强教授:研究指导、论文修改。
参考文献(略)
高飞,李惠凯,冯秀雪,等.3%聚桂醇消融动物囊性肿瘤模型的有效性和安全性研究[J/CD].中华胃肠内镜电子杂志,2023,10(1): 31-36.