《中华胸部外科电子杂志》2024 年 11 月第 11 卷
第 4 期肺切除术后支气管胸膜瘘诊疗进展
游雨禾 马钰杰 曹文军 薛洪省 朴哲 由茂端 史晓宇 赵志龙
作者单位:116601 大连,大连大学附属中山医院胸外科通讯作者:赵志龙,Email:zhilong509@126.com
摘要:支气管胸膜瘘(BPF)是肺切除术后的罕见且危及生命的并发症,是支气管和胸膜腔之间形成的异常通道。BPF可使气体和分泌物在余肺与胸腔内进行交换,引起咳嗽、胸闷气短,导致肺炎、脓胸、甚至张力性气胸等并发症的发生。因为BPF发病率低、成因复杂、形式多样等因素,所以相关诊疗研究较少,多为个案。本综述结合国内外相关研究报道,对术后BPF诊治方法及预防做一介绍,以期提高对其的认知与重视。
【关键词】 支气管胸膜瘘; 诊断; 治疗
DOI:10.3877/cma.j.issn.2095-8773.2024.04.07
支气管胸膜瘘(bronchopleural fistula,BPF)是指支气管与胸膜腔之间形成的异常通道,是一种罕见且危及生命的并发症。肺部切除术是BPF的主要成因,其他成因还有侵袭性感染或炎症、恶性肿瘤、创伤、自发性气胸、射频消融、急性呼吸窘迫综合征、机械通气等[1-2]。据统计,肺切除术后BPF发生率0.4%至4.5%,个别报道最高可至20%,其病死率最高可达到71%[3-5]。近年来,随着对疾病的认识和诊疗能力的提高,其病死率已降至4.6%[6]。
为了进一步降低术后BPF的发生率及病死率,临床医生需提高对其认识。在出现相关症状时,能尽快进行有针对性的措施和辅助检查,来准确定位和及时闭合瘘。目前,针对BPF的治疗措施主要包括保守治疗、手术干预和支气管镜介入治疗。本文将对肺切除术后BPF诊治方法及预防做一介绍,以期提高对其的认知与重视。
一、肺切除术后BPF的危险因素
肺癌术前新辅助放化疗及免疫治疗、合并肺部其他疾病、糖尿病、长期使用类固醇、免疫功能和营养状态低下,以及手术切缘癌残留、支气管闭合金属钉或缝线过敏等因素均可影响组织愈合,增加肺切除术后发生BPF的风险[7-9]。
也有研究显示,右肺切除和右肺下叶切除是术后发生BPF的危险因素[4,6,10-12]。这可能是肺的解剖结构所致。右主支气管相较于左主支气管更粗更直,导致支气管残端的分泌物积聚增多。同时,右肺中叶支气管管腔较细,与中间干支气管角度接近垂直,咳嗽时可形成湍流,且中叶排除气流较小,因此排痰效果不佳,下叶支气管残端发生感染,从而导致BPF。此外,右肺支气管多仅有一条动脉供血,且清扫淋巴结时易受损,使得支气管残端易暴露于缺血状态;右主支气管上方无主动脉覆盖,导致右主支气管残端的张力较大,这些因素均可能是右全肺切除和右肺下叶切除术后BPF发生率高的原因。
一项荟萃分析结果揭示 , 在八项临床研究中,有六项研究表明肺切除术后的机械通气与BPF的发生存在显著关联[13]。因此,肺部手术后进行机械通气的患者,可能导致BPF的发生。
二、肺切除术后BPF的分类
根据BPF发生的位置,分为中央型和外周型。中央型BPF通常涉及较大支气管,即发生在胸膜腔与段以上支气管之间,通常由创伤或外科手术引起。外周型BPF则发生在较小支气管,即胸膜腔与段及段以下支气管及肺实质之间,通常由肿瘤、坏死、支气管扩张或医源性引起[14]。
根据发生时间,术后BPF分为早期(1~7天)、中期(8~30天)和晚期(>30天)。早期BPF症状通常是较为剧烈,当胸腔内的液体通过瘘管吸入残肺时,出现咳嗽咳痰、呼吸困难、血氧饱和度和血压下降,皮下或纵隔气肿,甚至可能发生危及生命的张力性气胸;中晚期BPF表现则相对隐匿,以消瘦、发热和乏力为主要特征[3,6]。
三、肺切除术后BPF的诊断
准确识别和定位对于BPF的治疗非常重要。肺切除术后BPF的体征和症状可多样和非特异性。在临床实践中,肺切除术后主要以反复出现胸闷气短症状为主,进行胸腔闭式引流术减轻症状,同时通过观察患者呼吸过程中胸腔引流管中是否有气泡逸出,来诊断是否存在BPF。
胸部CT是诊断支气管胸膜瘘的重要手段。若瘘口较大时,胸部CT扫描可清晰显示瘘口的大小及位置;若瘘口较小且隐匿时,观察到胸膜腔内新发气体、气体较前增多、新发气液平面,亦是诊断BPF有力指标[2]。当多层螺旋CT结果显示胸膜增厚、残腔内分隔及积液时,通过多平面重组重建能明确瘘口位置和特征、胸膜状况,可以早期明确BPF的诊断[15]。
支气管镜检查在诊断BPF中也发挥重要的作用。大部分中央型BPF可在支气管镜下被观察到;对于外周BPF可在辅助球囊闭塞下识别定位,但此方法较为麻烦耗时[16]。吴晓东等[17]经胸引管逆行滴注亚甲蓝到胸腔,通过镜下观察是否有蓝色液体来确定发生BPF的位置。但是,这种亚甲蓝逆行滴注到胸膜腔的方法不易识别多灶性BPF,而将支气管内瓣膜反向放置并结合逆行亚甲蓝滴注可定位多灶性BPF。Xu等[18]采用此方法确诊了2例患者。
四、肺切除术后BPF的治疗
肺切除术后BPF的治疗分为保守治疗、手术、和支气管镜下介入治疗等。目前,BPF的治疗没有统一标准。在治疗时,需要根据瘘口直径、患者自身状况及对治疗后反应等因素,采取个体化措施。
1. 保守治疗
对于无法耐受外科手术或早期瘘口直径相对较小(<3 mm)的BPF患者,可通过胸腔闭式引流来负压吸引,排除胸腔内部液体或气体、促进剩余肺组织复张。数字胸腔引流系统能够调节负压引流强度,并可早期观察到停止漏气现象,从而缩短胸腔引流时间和住院时间[19-20]。
由于术后胸部疼痛,部分患者排痰不畅,导致肺部炎症,可进一步影响瘘口愈合。为了加速肺部炎症的缓解、促进其愈合,在充分胸腔引流的基础上,抗生素使用和全面的营养支持也是必备的。对细小的瘘口,胸腔内注入高浓度葡萄糖、抗生素等溶液进行冲洗也被证明行之有效[5,20-21]。
Boudaya等[22]曾将11名身体状况良好、术后肺扩张充分、且肺感染明显改善的BPF患者纳入为研究对象,经过充分的胸腔闭式引流及胸腔抗生素冲洗之后,9位患者成功实现愈合,仅有两名患者因为脓胸无法得到控制,最终接受手术治疗。
对于术后BPF且呼吸功能不全患者,需借助于机械性通气技术,精确地调节潮气量、呼吸频率以及气道阻力,可降低气道内气流速度,进而减轻对肺组织的损害达到一定治疗效果[23]。
2. 介入治疗
近年来,随着支气管镜技术的发展,其在BPF介入治疗中的应用已被证实为安全有效且微创,逐渐取代了大部分的手术治疗[10]。目前,对于有手术禁忌症、预后不良的基础疾病的BPF患者,临床上多选择支气管镜下介入治疗[24-25]。
然而,针对瘘口直径大小选择何种支气管介入治疗没有统一标准。临床多以5 mm为分界点,针对不同直径的瘘口采取不同治疗策略,有效率可达到66.7%至96.6%[6,10,26-28]。
针对瘘口直径较小(<5 mm)的BPF,尤其在≤3 mm的情况下,使用硬化剂或化学药物封堵剂都能取得良好疗效[26,29]。瘘口直径较大(≥5 mm)的BPF采用气管支架、支气管单向活瓣或心脏封堵器治疗可展现出较好的疗效[3,30-31]。
(1)硬化剂聚桂醇是一种合成聚乙二醇,其主要作用原理在于通过对静脉或毛细血管内膜的破坏,引发内皮细胞损伤,进而造成静脉壁纤维化,以实现对静脉或毛细血管的闭塞,从而达到硬化的效果[32]。由于其在食管-胃底静脉曲张的临床应用价值及安全性得到验证,随后被广泛用于瘘口封堵、血管瘤、囊肿和内痔的治疗,并取得了显著效果[33-34]。
支气管镜下注射聚桂醇等硬化剂已逐渐成为治疗BPF的主要手段之一,并且得到了多项研究的支持[10,25-26]。通过在瘘口周围注射硬化剂,使得围绕瘘口的支气管粘膜产生局部水肿,瘘口缩小甚至消失,显著减少胸腔引流的气体量。但随着水肿减轻,瘘口可再次出现,同时胸腔引流的气体增加。随后,硬化剂注射部位将发生黏膜下炎症反应和局部组织增生,从而导致瘘口缩小甚至闭合。局部组织增生在一周左右达到高峰。若瘘口仍未闭合,需再次通过支气管镜下注射硬化剂治疗[35-36]。
李洋等[26]通过支气管镜在瘘口周围黏膜多点注射聚桂醇治疗BPF,其成功率达到81.8%,同时也显示了聚桂醇治疗较小的中央型BPF具有显著效果。该文献也报道了2例瘘口直径较大(直径为12 mm瘘口),经一次注射治疗即治愈的情况。从而临床上对于较大的瘘口也可尝试注射硬化剂治疗,避免二次手术。
目前,针对聚桂醇治疗BPF的不良反应没有相关文献报道,但其在治疗其他疾病时,可出现皮肤色素沉着、局部组织缺血或血栓形成、低热、局部疼痛、头晕呕吐或迷走神经兴奋症状等不良反应,以及因注射不当,而损伤邻近血管,导致组织坏死[25,32,37]。
综上,对于不同直径的支气管胸膜瘘,硬化剂注射治疗均有一定疗效,尤其对于较小瘘口的治疗效果更为显著,且更为安全。
(2)封堵器对于瘘口直径≥5 mm的BPF患者,使用气道支架、支气管单向活瓣或心脏封堵器等治疗是一种可行的选择。
①气道支架:在一些呼吸道疾病的治疗中,气道支架具有极其重要的作用。在短期内,其能迅速修补瘘口、重建气道,恢复病变气管、支气管的完整性,进而改善患者生活质量[38]。
目前,临床上使用最广泛的气道支架是金属覆膜支架和硅酮支架,金属覆膜支架以镍钛合金为代表,具有优异的弹性和支撑性,置入过程简便,但可能引起肉芽组织增生,增加后期支架的移除难度;而硅酮支架则生物相容性好、柔软、可塑,但稳定性较差,易发生迁移,且置入较为复杂,可能导致管壁增厚狭窄,易发生黏液阻塞[30]。
使用气道支架治疗BPF时,需要考虑瘘口大小、位置和患者的具体情况。一项研究纳入了?148例肺部切除术后BPF患者,根据患者胸部CT、支气管镜等检查来定制金属支架。首次介入下放置金属支架成功率为96.6%(143例患者成功闭塞了瘘管),胸腔闭式引流无气泡溢出。随访30天后,141例患者复查后显示症状缓解,有5名患者死亡[39]。
有研究者通过对硅酮支架进行加工,使其更加适合患者瘘口相关支气管,可减少并发症的发生。该研究将其运用于17例BPF患者,术后16例患者成功置入支架后漏气现象立即消失,呼吸道症状均得到缓解。其中1例未成功置入,由于闭塞分支与气道之间的匹配失败[40]。
在某些情况下,硅酮支架和金属支架可以结合使用,这种方法被称为“杂交支架”治疗。采用Y形硅酮支架维持中央气道通气,金属支架则放置在Y形硅酮支架的远端,以重建气管到主支气管远端的气道并密封瘘口。该治疗策略可以迅速缓解呼吸困难症状,有效控制BPF相关的感染,同时二者互补增加稳定性,降低了支架的移位。研究中没有支架置入相关死亡及严重并发症[41]。
然而,这些支架最终需要移除,使患者再次受到侵入性操作。因此,生物可降解气道支架的研究有必要性。目前,生物可降解聚合物和生物可降解合金制造的气道支架已进入临床研究[42]。与标准金属和硅酮相比,生物可降解支架具有更好的生物相容性和更低的并发症[43]。
②支气管单向活瓣(endobronchi alvalve,EBV):EBV最初被用于慢性阻塞性肺疾病肺气肿的治疗,其可阻挡气流进入肺叶,有效减小靶肺容量,进而改善患者的呼吸功能[44]。作为一种单向吸气阻断设备,EBV可以使胸腔内的空气仅能流出而无法进入,同时有助于分泌物的排出,促进肺的复张,从而加速瘘口的愈合[45]。
近些年,支气管镜下EBV治疗BPF的方法得到了广泛认可,并取得了显著疗效。一项针对周围型BPF患者的回顾性研究显示,共有33名患者接受了支气管镜下置入EBV的治疗,其中22名患者的瘘口成功封堵,且这些患者均安全地将EBV取出,治疗有效率达66.7%至73.1%[27-28]。
EBV置入术后可能出现肉芽组织增生、感染、EBV脱落或位置移动等并发症,且所需医疗费用也相对较高[31]。为了尽可能地降低这些并发症的风险,有研究建议在EBV置入后的4~6周内,或者当患者不再出现漏气症状时,应考虑将EBV取出[1]。因其为侵入性操作,目前对于瘘口愈合后是否摘除EBV以及摘除时间,仍存在争议。
③心脏封堵器:心脏封堵器通常用于封堵心脏内部的缺损,如室间隔或房间隔缺损,是一种由镍钛合金金属丝网和多聚乙酯薄膜制成的自我扩张装置,可经内窥镜展开以堵塞瘘口。其中多聚乙酯薄膜被用作阻流膜,以确保封堵效果并促进肉芽组织生长及瘘口愈合,同时亦不会影响患者的排痰功能[46]。心脏封堵器具有较好的生物相容性、弹性、气密性,且尺寸可个性化,于是将其尝试用于治疗BPF[3]。
谭建龙等[47]的回顾性研究显示,16例术后中央型BPF患者采用支气管镜下置入房间隔缺损封堵器,其中15例患者成功封堵,经过长期随访,12例患者达到临床完全缓解。另有研究证明,经支气管镜下置入心脏封堵器治疗BPF的疗效和安全性较好[48-49]。
然而,由于气道与心脏的解剖结构、生理化学环境,以及力学特性存在较大差异,置入心脏封堵器可出现位移、脱落和气道狭窄等并发症。使得将其用于BPF治疗存在一定争议[50]。因此,未来有必要改进该装置,使其更适应气道环境,为患者提供更为安全的治疗手段。
(3)间充质干细胞(mesenchymal stem cell,MSC)MSC作为一种具有自我更新与多谱系分化潜能的未分化干细胞,主要可分为胚胎干细胞与成体干细胞两大类别。其中,成体干细胞可从脂肪组织、外周血、骨髓等组织中获取[51]。
MSC具备免疫调节与抗炎特性,并能规避宿主免疫系统,从而实现同种异体移植。移植后的MSC通过与受损组织或器官内的邻近微环境相互作用,促进组织愈合、修复乃至潜在的再生[52-53]。
随着MSC的应用范围日益广泛,已有研究将其应用于BPF的治疗,术后瘘口愈合情况良好,临床症状亦有所缓解[54]。
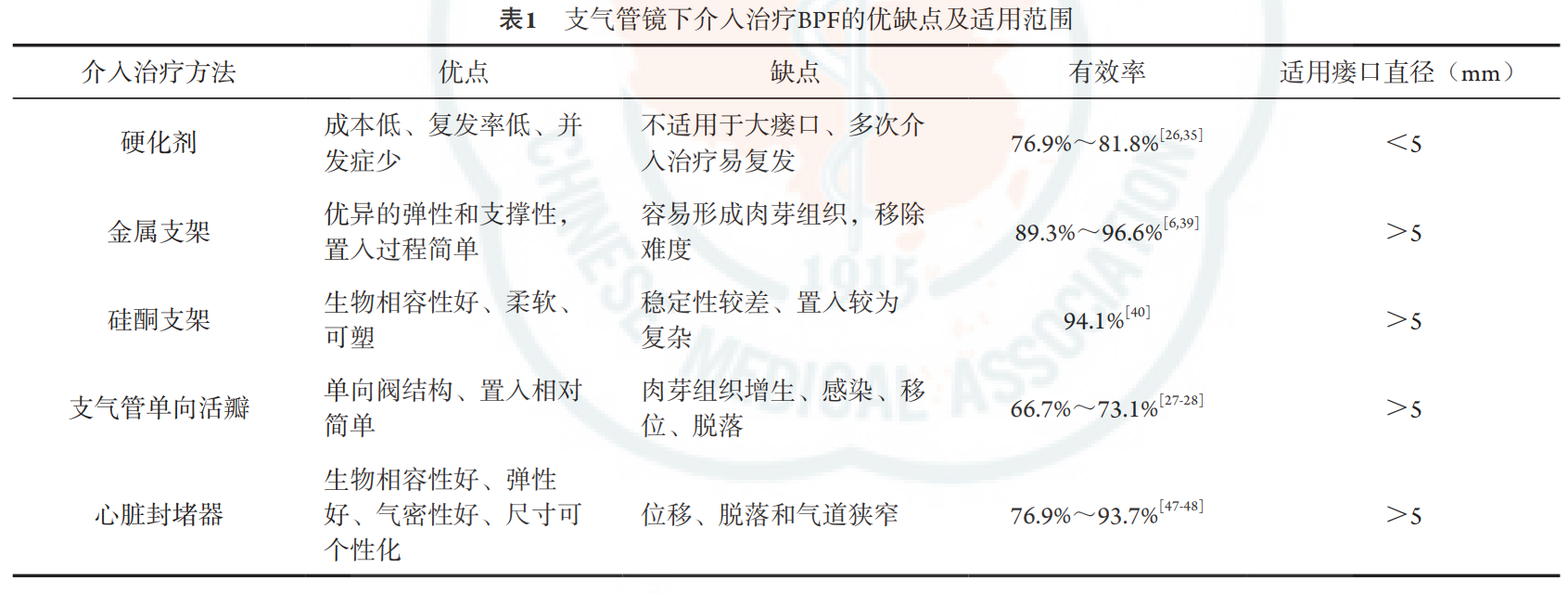
Marchioni等[55]采用自体腹膜脂肪移植结合合成胶与透明质酸进行BPF的内镜下修补,脂肪团成功封堵后漏气立即停止,随访3个月仍保持闭合状态。然而,该研究亦指出,随着时间推移,无血供的脂肪细胞会出现坏死与凋亡,导致移植物逐渐缩小,再次出现瘘口的可能。支气管镜下介入治疗皆有利弊,MSC治疗亦不例外。截至目前,MSC用于BPF的临床应用较少,缺乏数据证明其疗效。根据现有证据,将各种介入治疗的优缺点及适用范围进行了整理,详见表1。
3. 手术治疗
对于早期、瘘口直径较大(>8 mm)或非手术治疗无效的患者,可以考虑手术进行干预[25]。
然而,手术治疗创伤较大,且瘘口仍有复发风险,并可能出现严重并发症甚至死亡,因此,术前应充分评估[3,6]。
手术方式主要是通过对支气管残端进行加固缝合或再次切除吻合口,经测试无漏气,确认BPF修复完好后,可采用心包、肋间肌瓣、大网膜等血运丰富的组织加固残端[56]。
大网膜不仅有丰富血运,还具有大量淋巴管,能够参与抗原识别和免疫反应,具有强大的抗感染能力、吸收液体和促进局部血管生成等优点,从而促进组织或瘘口愈合。杨晓樽等通过心膈角处打开膈肌获取大网膜治疗BPF,6例患者均在一次修补术后瘘口愈合,随访无复发。叶亮等将5例患者通过腹腔镜获取移植修补,5例患者均未出现消化道不良反应,其中有1例患者因大网膜液化坏死而行二次修补,其余患者愈合良好[57-58]。因此,大网膜在修补BPF显示出了较好的疗效及安全性。
肋间肌瓣具有良好的血液供应,组织厚度适中,可提供足够的组织以加强和修补支气管残端;且与手术区域较近,可在同一手术过程中方便制备,而其他肌瓣的获取创口较大[59]。该手术方式沿着切口上一肋骨上缘紧贴肋骨骨膜精细分离,保持壁层胸膜的完整性,并根据瘘口直径的大小获取含血管神经蒂的肋间肌瓣,再将其缝合包盖支气管残端。
杨继承等[60]采用带蒂肋间肌瓣治疗7例全肺切除术后早期BPF患者,4例Ⅰ期愈合,3例患者出现发热等感染症状,予以胸腔注药、抗感染后好转,随访无复发。何忠良等[61]采用肌瓣或肌皮瓣治疗术后难治性脓胸合并BPF患者15例,肌瓣成活率93.33%,中期治愈率86.67%。其中1例患者因肿瘤转移死亡。采用肌瓣填塞或修补支气管残端时,须注意动静脉血供和肌瓣的活力,避免其坏死而出现BPF复发。
有研究[62]将大网膜与肌瓣修补BPF进行了比较,显示出肌瓣修补者复发率和病死率较高、并发症更多,从而住院时间延长。可能原因为大网膜具有较好的抗炎特性,从而胸腔内较为清洁,保持良好的愈合条件,肌瓣组织选择不当可使血供受限,导致修补失败。
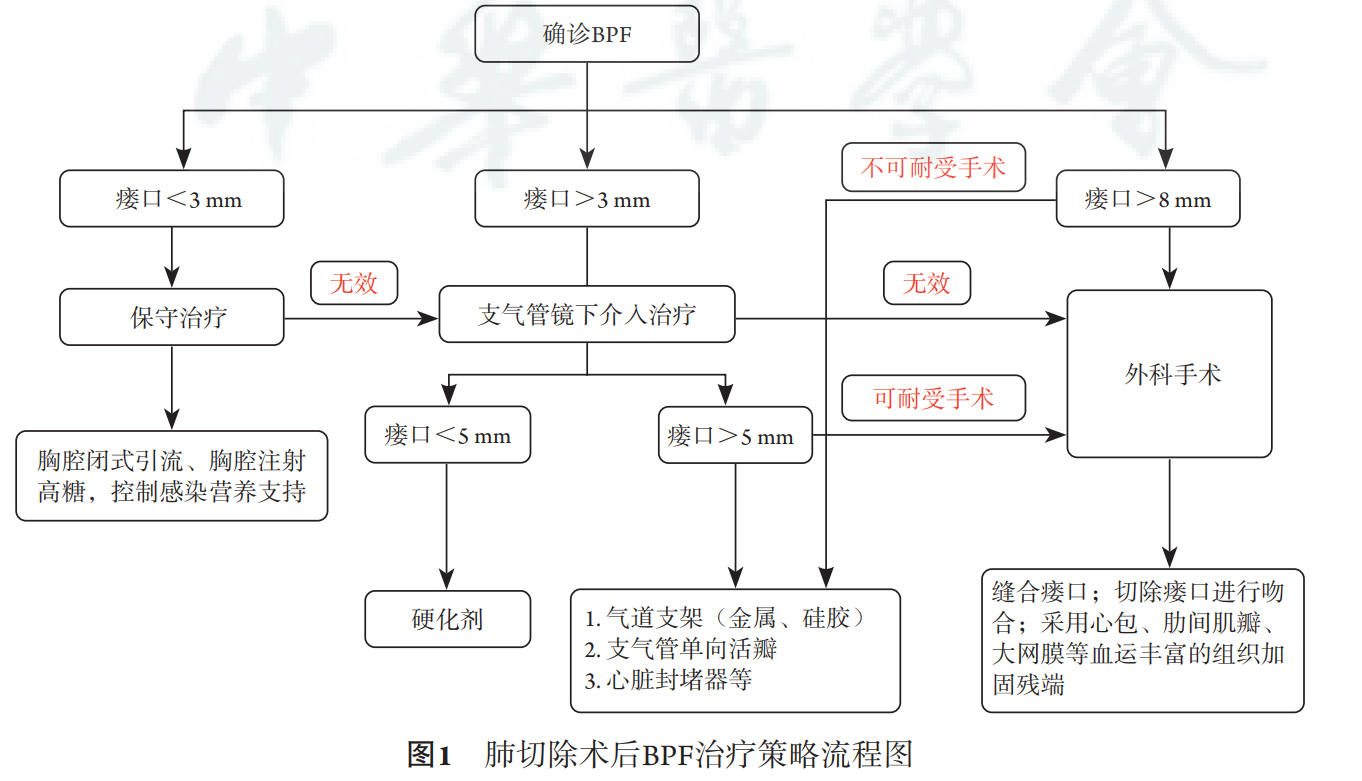
在临床工作中,结合既往的诊疗经验以及国内外研究文献,针对肺切除手术后BPF的治疗策略形成了一个流程图,见图1。
五、预防
肺切除术后引发的漏气现象是导致住院周期延长的关键因素,亦可能出现脓胸,并成为其他危重且影响生命安全的并发症的源头。因此,预防此类疾病的发生有着极其重要的意义。可分为术前、术中及术后3个阶段的预防。
术前阶段应对患者进行全面的评估和处理,如戒烟、纠正患者的营养不良和贫血等常见全身问题,减少类固醇的使用以防止伤口愈合延缓。术中注意精细操作,清扫淋巴结时,注意保护支气管动脉,避免损伤支气管残端及其周围肺组织的供血血管;同时选择合适的吻合钉仓,避免支气管残端张力过大及支气管残端过长,以<3 mm为最佳,闭合后应仔细检查残端是否存在漏气现象,必要时可加固缝合,还可采用生物蛋白胶、富含血供的组织(如肋间肌瓣、大网膜等)来包裹支气管残端。术后阶段则需确保充分引流、合理运用抗生素治疗、以及支气管分泌物及时有效的清理[63-64]。
六、展望
随着设备技术的不断进步,使用支气管镜介入治疗可能会在BPF的综合管理中发挥越来越重要的作用,为患者提供有效的微创解决方案,支气管镜下介入治疗有可能为传统的外科手术提供侵入性更小、对患者更友好的替代方案。但支气管镜下各种治疗方案仍存在一定程度上的缺陷与挑战,需要对其进一步研究,建立标准化治疗方案,完善材料选择标准,并加强对患者的长期监测,以期实现对肺切除术后BPF诊疗的优化与完善。