《浙江临床医学》2020年6月第22卷第6期
α-糜蛋白酶联合聚桂醇在甲状腺粘滞性囊性结节中的应用
彭玲耀 司星 傅晓凤 朱江
【310016 浙江大学医学院附属邵逸夫医院(彭玲耀 傅晓凤 朱江)318020 浙江省台州市第一人民医院(彭玲耀)310018 杭州师范大学医学院(司星)】
摘要:
目的:研究α-糜蛋白酶联合聚桂醇在甲状腺粘滞性囊性结节中的应用价值。
方法:60例甲状腺粘滞性囊性结节随机纳入观察组和对照组,观察组(36例)采用0.9%氯化钠溶液混合α-糜蛋白酶冲洗囊腔,再用聚桂醇硬化治疗,对照组(24例)抽吸囊液后采用聚桂醇硬化治疗。
结果:治疗后囊腔体积明显变化,观察组有效率为91.7%,对照组有效率为66.7%,差异有统计学意义(P<0.05)。
结论:α-糜蛋白酶联合聚桂醇治疗甲状腺粘滞性囊性结节安全有效,能提高聚桂醇硬化治疗效果。
关键词:
α-糜蛋白酶,聚桂醇,甲状腺粘滞性囊性结节
随着超声技术不断发展及健康体检日益普及,甲状腺结节检出率不断增加。据报道,良性结节检出率20%~76%,其中囊性结节或以囊性为主的良性结节达15%~30%[1],超声引导下聚桂醇硬化治疗囊性结节微创、有效、美观。但部分结节囊液极其粘稠,18G 针难以抽吸或抽出液体量 <0.5ml,此类结节被称为甲状腺粘滞性囊性结节[2],这种高粘度囊液难以抽取并抑制硬化剂的扩散导致硬化效果减弱或失败[2-3],α- 糜蛋白酶联合聚桂醇硬化治疗此类结节取得了良好效果,现报道如下。
一、资料与方法
1.1 一般资料
连续选取 2016 年 1 月至 2018 年 6 月在本院就诊的甲状腺粘滞性囊性结节 60 例,其中男19 例,女 41 例,年龄 20~85 岁。随机分配纳入观察组和对照组,观察组 36 例,对照组 24 例。纳入标准:(1)结节选取单纯囊性或实性部分 <20%、囊性部分18G 穿刺针难以抽吸或抽出液体量 <0.5ml ;(2)结节确诊良性(穿刺病理证实);(3)有临床症状或美容需求要求治疗。排除标准:(1)严重心肺肾功能不全;(2)凝血功能障碍、1 周内服用抗凝血药物 ;(3)超声有恶性征象或病理学检查可能恶性患者。所有患者均签署知情同意书,此研究经过浙江省邵逸夫医院伦理委员会讨论同意。
1.2 仪器和方法
应用 LOGIC E9 彩色多普勒超声诊断仪,频率 9~16Hz。聚桂醇 :陕西天宇制药有限公司生产的聚桂醇注射液,规格含量为 10ml ∶ 100mg。穿刺引流针 :北京德迈有限公司的介入穿刺针,规格 :16G/11cm。糜蛋白酶 :上药第一生化药业有限公司生产,规格 :4000U/ 瓶。
1.3 治疗方法
患者仰卧位,颈部向后伸展,充分暴露。术前对甲状腺进行全面检查,观察甲状腺结节大小、形态、数量、位置、内部囊实性占比、血流分布情况、与周围组织关系,并规划穿刺方案。常规消毒铺巾,穿刺部位皮肤局部浸润麻醉(采用 2% 利多卡因),超声引导下将穿刺针进至囊性结节中心,确定针尖位置,接注射器及引流管,观察组多点缓慢注入 α- 糜蛋白酶稀释液(由 0.9%10ml 氯化钠溶液与 4000Uα- 糜蛋白酶混合,注入量为原囊液体积的 20%),20min 后,边注射边冲洗,反复冲洗,尽量抽尽囊液后,注入原囊性体积 1/2 量聚桂醇反复冲洗,并保留 9min 后全部抽出,注入事先制备聚桂醇泡沫(原液 / 空气比 =1/4)保留,保留量为原囊液体积 1/3。对囊实性结节在实性部分内多点注入少量聚桂醇原液。术毕聚桂醇原液封闭针道,拔针后压迫约 10min,观察 1h。对照组单纯抽吸囊液后,聚桂醇硬化治疗步骤与观察组一致。
1.4 观察指标
术中、术后观察患者有无不良反应,术后于 1、3、6、12 个月进行随访。记录结节大小、容积及缩小率、症状评分、美容评分。容积 = 上下径× 前后径 × 左右径 ×0.52,径线使用 cm 为单位,容积单位 ml ;容积缩小率 =(术前容积 - 术后容积)/ 术前容积 ×100%,容积单位 ml;美容评分标准:1 分:无可触及肿块 ;2 分 :可触及但不可见 ;3 分 :仅在吞咽时可见 ;4 分 :轻易可见。症状评分标准 :使用直观模拟卡尺法,患者根据症状的强度及心理上的感受能力将游标推至相应位置评分[4]。治疗有效 :术后囊腔体积缩小 >50%。
1.5 统计学分析
采用 SPSS 20.0 统计软件。计量资料以(-x±s)表示,组间比较采用 t 检验,P<0.05 为差异有统计学意义。
二、方法
2.1 治疗前后体积变化
两组囊性结节体积在治疗前无明显差异(P>0.05),术后 1、3、6、12 个月随访残存体积观察组缩小明显优于治疗组,两组变化差异明显(P<0.05),见表1。观察组治疗前后超声图见图 1~3。
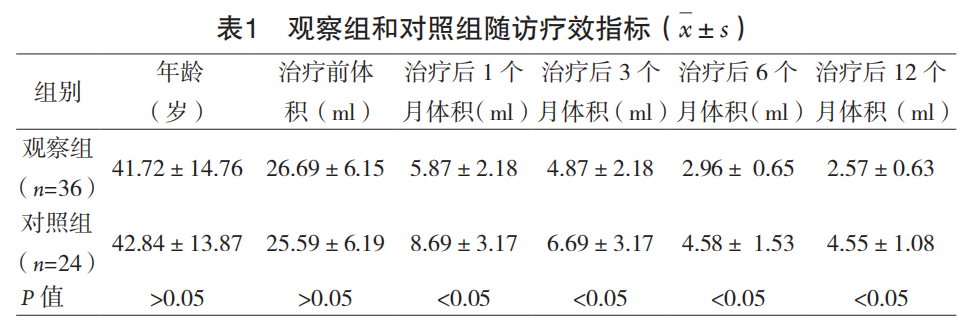
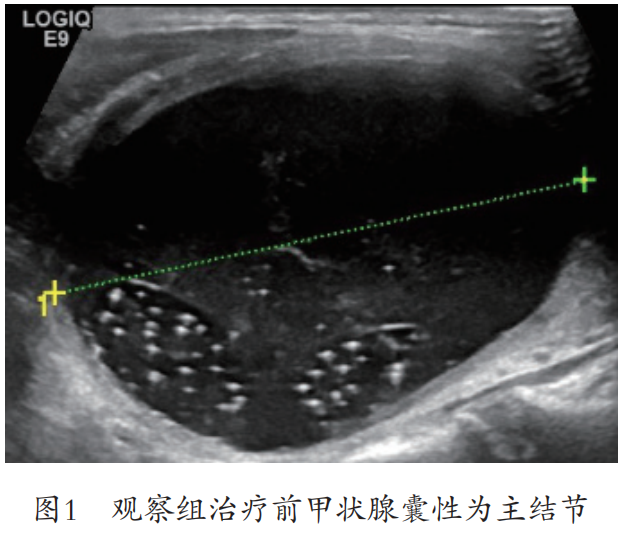
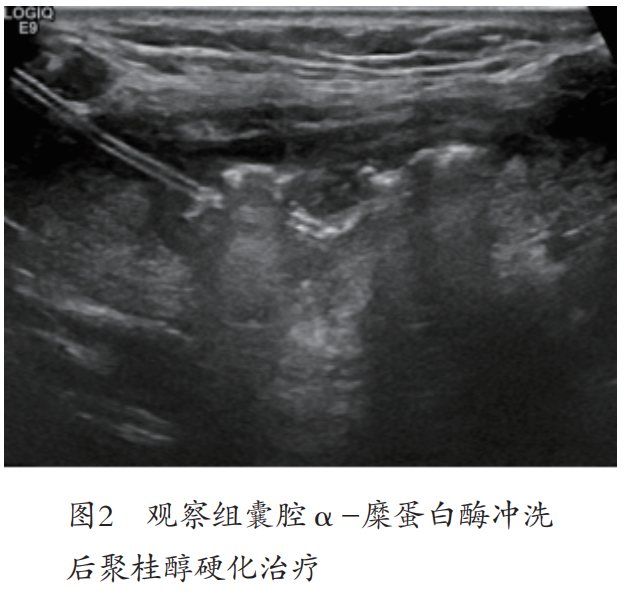
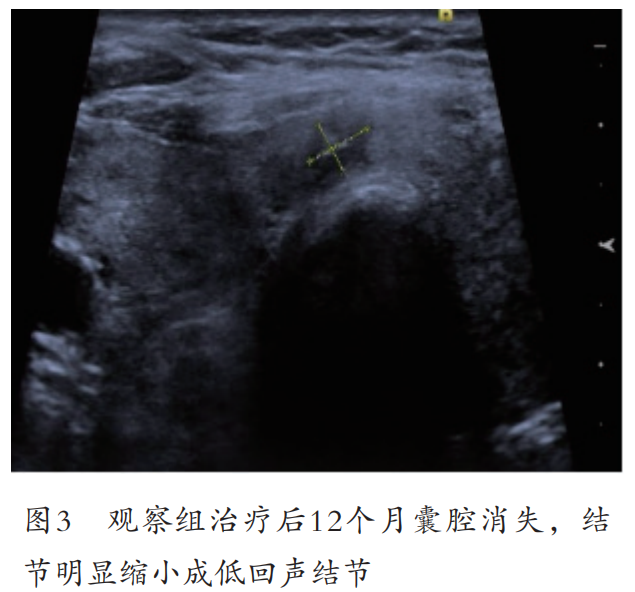
2.2 疗效评估
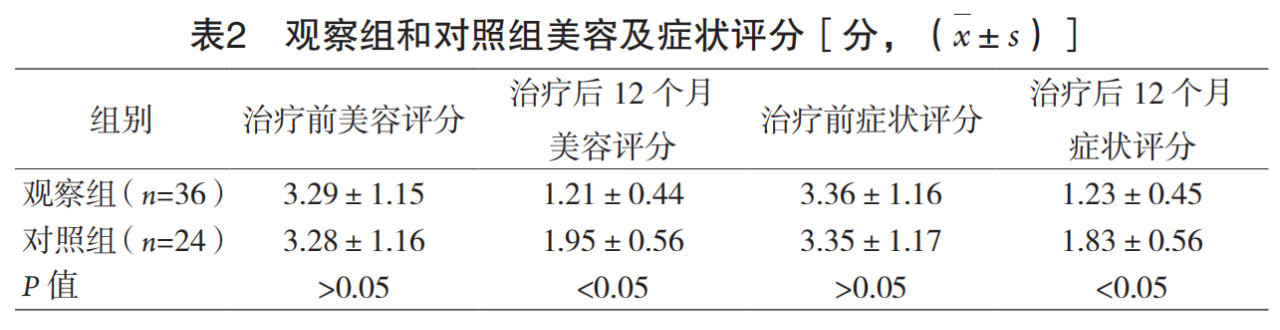
观察组术后1、3、6、12 个月随访症状评分及美容评分改善明显优于对照组(P<0.05), 见表2。治 疗后 12 个月随访,观察组有效 33 例, 无效 3 例,对照组有效 16 例,无效8 例,观察组治疗有效率显著优于对照组(91.7% vs. 66.7%,P<0.05)。
2.3 不良反应
超声引导下 α- 糜蛋白酶冲洗过程中未出现明显不良反应,聚桂醇硬化治疗不良反应轻微,观察组 2 例,对照组 1 例出现一过性发热,体温<38.5℃持续时间 <2d,未经特殊治疗好转。未发现其他严重并发症。
三、讨论
甲状腺囊性结节经超声引导硬化治疗疗效显著,但部分结节因囊液为胶质成分或囊液过分粘稠而治疗失败,这类粘滞性囊性结节约占所有甲状腺囊性结节的 30%[2],治疗效果差,复发率高,国内外文献报道此类结节建议手术治疗[5-8]。外科手术不仅有麻醉风险,术后并发症多,且切口疤痕影响美容美观。影响超声引导硬化治疗效果的关键因素之一是能否将囊液抽吸彻底,其一 :残留囊液稀释硬化剂,不能达到有效浓度从而影响硬化效果,有文章报道不同浓度的聚桂醇在子宫内膜异位囊肿中起到不同效果[9];其二 :粘稠的囊液附在囊壁上,会影响硬化剂接触囊壁,从而减弱了硬化剂对囊壁上皮细胞的灭活作用,残存囊壁上皮细胞分泌囊液,导致结节复发[10];其三 :粘稠的囊液与硬化剂发生凝固作用,影响硬化剂弥散,并易堵塞穿刺引流针,导致硬化失败[11]。如何彻底吸除囊液成为关键技术之一,国内外主要有以下几种方法:(1)采用开槽式或较粗孔径引流针,对胶质囊肿取得一定的效果,但对粘稠的巧克力样结节仍不能彻底抽吸。(2)在结节内注入无水酒精或聚桂醇,7~14d 后再进行硬化治疗,取得不错的效果,但是因时间跨度大,需要进行两次操作,增加了患者的经济及心理负担。(3)在囊性结节内注入α- 糜蛋白酶进行溶解冲洗,取得了良好效果[12]。本资料中观察组采用第三种方法对囊腔进行冲洗,α- 糜蛋白酶是一种来自于动物胰腺的生物蛋白酶,类似于胰蛋白酶,却比胰蛋白酶分解蛋白质作用更强、但毒性低,不良反应更少。蛋白酶对粘稠囊液主要起了溶解变性蛋白质,纤维组织及分泌物的作用,逐步溶解粘稠囊液[13],囊腔冲洗干净后再进行聚桂醇硬化治疗,使得有效浓度的聚桂醇硬化剂充分与囊壁接触从而更好地发挥硬化作用。
硬化剂种类繁多,使用较为广泛主要为无水乙醇及聚桂醇。但目前国内无水乙醇供货链断裂,缺乏用于人体内的制剂,且无水酒精的不良反应颇多,包括疼痛、醉酒样反应,体内应用对人体脏器存在潜在风险。聚桂醇注射液是由十二醇经乙氧基化产生的,化学名聚氧乙烯月醇,具有止血、硬化作用。在国外已有数十年的治疗历史,疗效肯定,未见明显不良反应。
综上所述,α- 糜蛋白酶联合聚桂醇硬化治疗甲状腺粘滞性囊性结节取得了良好的治疗效果,与对照组存在疗效差异,并且安全性好,不良反应少,有望成为甲状腺粘滞性囊性结节首选治疗方式。








