发布时间:2022-05-18 10:26:30 来源: 浏览次数:973
《药物评价研究》2022年5月第45卷第5期
聚桂醇局部注射联合马来酸噻吗洛尔治疗婴幼儿血管瘤的临床疗效
张均秀,齐 帅,高 磊
摘要:
目的:探讨聚桂醇局部注射联合马来酸噻吗洛尔治疗婴幼儿血管瘤的临床疗效。
方法:前瞻性选取2017年1月—2018年12月保定市儿童医院收治的血管瘤婴幼儿150例,采用信封法分为对照组(75例)和试验组(75例)。对照组给予马来酸噻吗洛尔治疗,将0.5%马来酸噻吗洛尔滴眼液用纱布湿敷在血管瘤部位及周围皮肤,早晚各1次,每次1 h。试验组给予马来酸噻吗洛尔滴眼液联合聚桂醇局部注射,马来酸噻吗洛尔滴眼液用法用量同对照组,聚桂醇局部注射方法:将聚桂醇注射液和空气按照1∶3比例混合,来回推注制成泡沫状硬化剂,制作完成后需尽快注射。也可直接注射聚桂醇原液,体积较小的血管瘤可进行单点注射;体积较大的血管瘤可进行多点注射。间隔1个月再注射1次,根据患儿情况治疗1~4个月。两组患儿均随访6个月,根据患儿恢复情况决定是否继续用药。分别于治疗前和治疗后采用视觉模拟评分(VAS)评估瘤体颜色及大小,比较两组患儿治疗前和治疗后血管瘤厚度及治疗时间,比较两组患儿治疗前和治疗后血清细胞因子[缺氧诱导因子-1α(HIF-1α)、血管内皮生长因子(VEGF)、表皮生长因子样结构域(EGFL7)、基质金属蛋白酶-9(MMP-9)]水平,记录两组不良反应发生率及临床疗效。
结果:治疗前两组患儿血管瘤厚度比较,差异无统计学意义(P>0.05);治疗后两组患儿血管瘤厚度均较治疗前明显降低(P<0.05),且治疗后试验组瘤体厚度明显低于对照组(P<0.05);试验组治疗时间明显短于对照组(P<0.05)。治疗前两组患儿血清HIF-1α、VEGF、EGFL7、MMP-9水平比较,差异无统计学意义(P>0.05),治疗后两组患儿血清HIF-1α、VEGF、EGFL7、MMP-9水平均较治疗前显著降低(P<0.05),且治疗后试验组血清HIF-1α、VEGF、EGFL7、MMP-9水平显著低于对照组(P<0.05)。治疗前两组患儿血管瘤大小及颜色VAS评分比较,差异无统计学意义(P>0.05);治疗后两组患儿血管瘤大小及颜色VAS评分均较治疗前显著升高(P<0.05),且治疗后试验组血管瘤大小及颜色VAS评分显著高于对照组(P<0.05)。试验组总不良反应发生率6.67%,与对照组总不良反应发生率(9.33%)比较,差异无统计学意义(P>0.05)。试验组总有效率为93.33%,对照组的总有效率为74.67%,试验组总有效率显著高于对照组(P<0.05)。
结论:马来酸噻吗洛尔联合聚桂醇局部注射治疗婴幼儿血管瘤临床效果较好,不良反应少,并且能够缩短治疗时间。
关键词:
马来酸噻吗洛尔;聚桂醇;婴幼儿血管瘤;缺氧诱导因子-1α;血管内皮生长因子;表皮生长因子样结构域;基 质金属蛋白酶-9
婴幼儿血管瘤是一种良性肿瘤,在婴幼儿中比较常见,多发生于头面颈部,病程较长,严重影响患儿容貌[1]。虽有些血管瘤能够自行消退,但为了防止一些增殖较快、面积较大的血管瘤引起皮肤溃疡、出血感染等风险,还应早期进行治疗[2]。目前,血管瘤临床治疗手段主要有外用药物、口服激素、局部注射或激光治疗等方式,但激光治疗对于消退期血管瘤比较有效,而对于增生期血管瘤效果不明显。马来酸噻吗洛尔属于非选择性β受体阻滞剂,是近年来发现的对于婴幼儿血管瘤疗效较好的药物[3],但单独使用效果较慢。聚桂醇是一种硬化剂,最初被用于静脉曲张的治疗,近些年被用于婴幼儿血管瘤治疗中,也具有较好的效果[4]。本研究将马来酸噻吗洛尔与聚桂醇局部注射联合用于婴幼儿血管瘤的治疗,观察其对血管瘤厚度及治疗时间、血清细胞因子水平、瘤体颜色及大小的影响,观察其不良反应发生率,为临床婴幼儿血管瘤的治疗和临床用药提供依据和参考。
一、 资料与方法
1.1 分组方法
采用信封法分组:预先准备150个不透明信封,对信封进行1~150编号,患者根据就诊顺序抽取,抽到1~75号的患者为对照组,抽到76~150号的患者为试验组。
1.2 一般资料
前瞻性选取2017年1月—2018年12月保定市儿童医院收治的血管瘤婴幼儿150例,男66例,女84例;瘤体直径0.5~5.0 cm,平均(2.01±0.33)cm;年龄1~12个月,平均(5.30±1.34)个月;发病时间1~3个月,平均(1.25±0.35)个月;病变部位:四肢17例、躯干35例、头面颈部98例;混合型血管瘤82例,浅表型血管瘤36例,深部型血管瘤32例。本研究经保定市儿童医院伦理委员会批准[2016(年)伦审【科】第(32)号],患儿家属均在治疗前签署知情同意书。
1.3 纳入标准和排除标准
1.3.1 纳入标准
①均符合《口腔颌面部血管瘤和脉管畸形治疗指南》[5]中血管瘤诊断标准;②发病后未接受过其他治疗;③血管瘤完好无溃疡;④年龄≤12个月。
1.3.2 排除标准
①患有先天性心脏病者;②合并全身感染者;③合并有湿疹者;④合并窦性心动过缓及房室传导阻滞者。
1.4 方法
两组患儿治疗前均行常规检查,包括生命体征、心电图、血常规、血压、血糖、肝肾功能等。对照组给予马来酸噻吗洛尔治疗,将0.5%马来酸噻吗洛尔滴眼液(武汉五景药业有限公司,国药准字H42021078,规格:5 mL∶25 mg,批号:20160514、20170620、20180325)用纱布湿敷在血管瘤部位及周围皮肤,每次1 h,早晚各1次。试验组给予马来酸噻吗洛尔滴眼液联合聚桂醇局部注射,马来酸噻吗洛尔滴眼液用法用量同对照组,聚桂醇局部注射方法:将聚桂醇注射液(陕西天宇制药有限公司,国药准字H20080445,规格:10 mL∶100 mg,批号:20160704、20170511、20180219)和空气按照1∶3比例混合,来回推注制成泡沫状硬化剂,制作完成后需尽快注射[6]。也可直接注射聚桂醇原液,体积较小的血管瘤可进行单点注射,用4~5号针头刺入瘤体最隆起处,回抽有血液后,将聚桂醇原液注入瘤腔至皮损稍发白为止;体积较大的血管瘤可进行多点注射,用4~5号针头在瘤体周围上下左右各点均注射1针,之后在瘤体中心注射1针,每点注射不超过1 mL。间隔1个月再注射1次,根据患儿情况治疗1~4个月,若患儿瘤体基本消退后,则减少聚桂醇注射液的用量,直至停药。两组患儿均随访6个月,根据患儿恢复情况决定是否继续用药。
1.5 观察指标
随访6个月,以打电话或门诊复查的方式进 行随访,每 2周随访 1次,观察并记录两组患儿瘤体 的厚度及治疗所用时间。(2)血清细胞因子[7] 测定: 分别抽取两组患儿治疗前及治疗4个月后空腹静脉血 5 mL,分离上层血清(3 500 r·min?1 离心 10 min), 采用酶联免疫法检测两组患儿血清缺氧诱导因 子 -1α(HIF-1α)、血管内皮生长因子(VEGF)、表皮 生 长 因 子 样 结 构 域 7(EGFL7)、基 质 金 属 蛋 白 酶-9(MMP-9)水平,其中HIF-1α试剂盒购自北京博 胜经纬科技有限公司,VEGF、MMP-9试剂盒购自北 京索莱宝科技有限公司,EGFL7试剂盒购自武汉菲 恩 生 物 科 技 有 限 公 司 。(3)采 用 视 觉 模 拟 评 分 法(VAS)对治疗前及治疗4个月后的血管瘤颜色及 大小进行评分[8],在纸上画 1 条长 20 cm 的直线,中 间为“0”点,左端为?10,右端为10,越向左代表瘤体 越大颜色越深,越向右代表瘤体越小颜色越浅。(4) 不良反应发生率:随访6个月,观察并记录两组患儿 出现色素沉着、色素减退、皮肤萎缩情况。(5)临床 疗效[9]:采用 Achauer 等[9] 提出的分级标准于治疗 4 个月后评估疗效。瘤体缩小≤25%,或表面颜色较 治疗前有所消退,即为Ⅰ级;25%<瘤体缩小≤50%, 或表面颜色明显消退,即为Ⅱ级;50%<瘤体缩小≤ 75%,且表面颜色明显消退,即为Ⅲ级;瘤体缩小> 75%,或表面颜色完全消退,即为Ⅳ级。
总有效率=(Ⅲ级例数+Ⅳ级例数)/总例数
1.6 统计学方法
数据均采用统计学软件 SPSS 20.0 进行分析, 符合正态分布的计量资料采用图片表示,采用样本 t检验进行组内及组间比较;计数资料采用百分率表 示,并行χ2 检验。P<0.05表示差异有统计学意义。
二、 结果
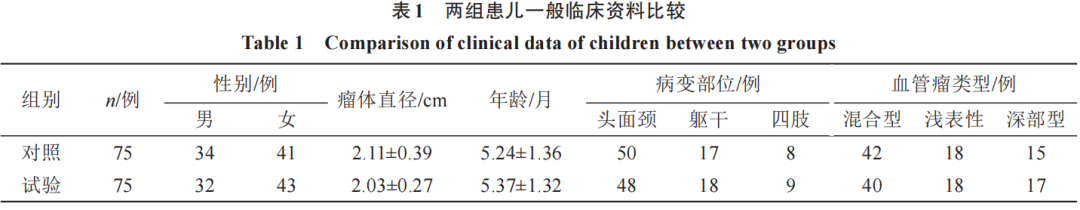
2.1 两组患儿一般资料比较
按照信封法将150例患儿分为对照组和试验组,每组各75例,试验过程中无脱落病例。两组患儿瘤体直径、年龄、病变部位、血管瘤类型等一般资料比较,差异无统计学意义(P>0.05),具有可比性。见表1。
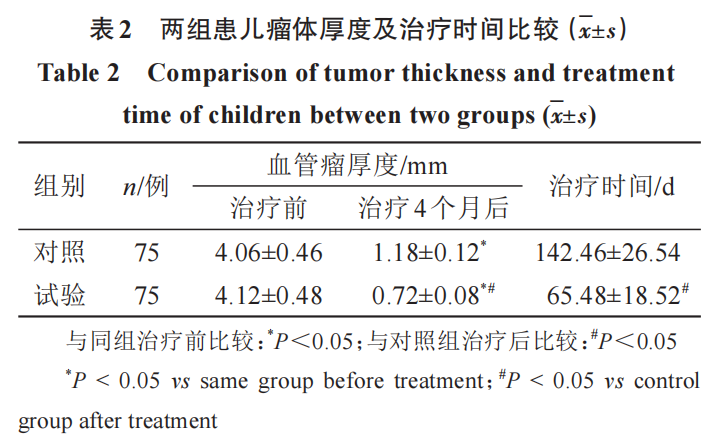
2.2 两组患儿瘤体厚度及治疗时间比较
治疗前两组患儿血管瘤厚度比较,差异无统计学意义(P>0.05);治疗后两组患儿血管瘤厚度均较治疗前明显降低(P<0.05),且治疗后试验组瘤体厚度明显低于对照组(P<0.05);试验组治疗时间明显短于对照组(P<0.05)。见表2。
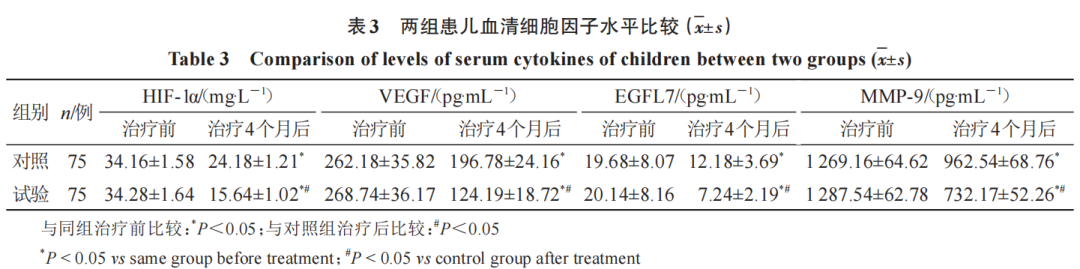
2.3 两组患儿血清细胞因子比较
治疗前两组患儿血清HIF-1α、VEGF、EGFL7、MMP-9水平比较,差异无统计学意义(P>0.05),治疗后两组患儿血清HIF-1α、VEGF、EGFL7、MMP-9水平均较治疗前显著降低(P<0.05),且治疗后试验组血清HIF-1α、VEGF、EGFL7、MMP-9水平显著低于对照组(P<0.05)。见表3。
2.4 两组患儿血管瘤大小及颜色VAS评分比较
治疗前两组患儿血管瘤大小及颜色VAS评分比较,差异无统计学意义(P>0.05);治疗后两组患儿血管瘤大小及颜色VAS评分均较治疗前显著升高(P<0.05),且治疗后试验组血管瘤大小及颜色VAS评分显著高于对照组(P<0.05)。见表4。

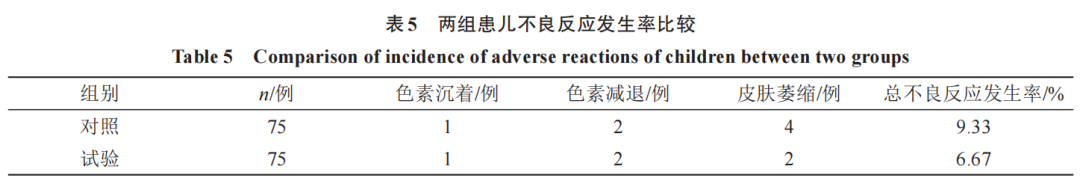
2.5 两组患儿不良反应发生率比较
试验组总不良反应发生率6.67%,与对照组总不良反应发生率(9.33%)比较,差异无统计学意义(P>0.05)。见表5。
2.6 两组患儿临床疗效比较
试验组总有效率为93.33%,对照组的总有效率为74.67%,试验组总有效率显著高于对照组(P<0.05)。见表6。

三、 讨论
婴幼儿血管瘤是1岁以下婴幼儿常发的良性肿瘤,虽大部分可自行吸收,但发展结果具有不可控性,仍有小部分患儿的血管瘤无法自行消退[10]。因此,应及早采取治疗措施,临床常用普萘洛尔来治疗婴幼儿血管瘤,普萘洛尔属于非选择性β受体阻滞剂,金芳等[11]研究结果显示,将普萘洛尔用于婴幼儿血管瘤中效果较好。马来酸噻吗洛尔是最强的非选择性β受体阻滞剂,作用效果是普萘洛尔的8倍[12],但单独使用治疗时间较长。聚桂醇是一种新型硬化剂,致敏性及毒性较低,可直接作用于血管瘤,使瘤体萎缩消失[13]。金轶等[14]研究结果显示,聚桂醇用于治疗婴幼儿血管瘤不管单独使用还是联合使用均具有较好疗效。本研究结果显示,试验组总有效率93.33%显著高于对照组的总有效率(74.67%),提示马来酸噻吗洛尔联合聚桂醇局部注射治疗婴幼儿血管瘤具有较好疗效,与金轶等[14]研究结果一致。
EGFL7是一个在血管内皮特异性表达的基因,对血管功能完善、管腔形成具有重要作用,HIF-1α是一种与血管生成有关的转录因子,可以促进新生血管形成,VEGF是血管内皮生长因子,能够促进血管内皮细胞增殖[15],MMP-9参与血管生成。本研究结果显示,治疗后两组患儿血清HIF-1α、VEGF、EGFL7、MMP-9水平较治疗前降低,且试验组低于对照组,提示马来酸噻吗洛尔联合聚桂醇局部注射通过下调HIF-1α、VEGF、EGFL7、MMP-9水平,来抑制血管瘤生长,从而使瘤体消退。治疗后,两组患儿血管瘤厚度明显降低,且试验组低于对照组,试验组治疗时间也短于对照组;治疗后两组患儿血管瘤大小及颜色VAS评分较治疗前显著升高,且试验组血管瘤大小及颜色VAS评分高于对照组,提示马来酸噻吗洛尔联合聚桂醇局部注射可以缩短治疗时间,较快改善血管瘤厚度、大小及颜色。试验组总不良反应发生率为6.67%,与对照组总不良反应发生率(9.33%)比较,差异不显著,提示马来酸噻吗洛尔联合聚桂醇局部注射不会增加患儿不良反应,较为安全。
综上所述,马来酸噻吗洛尔联合聚桂醇局部注射用于婴幼儿血管瘤中效果较好,不良反应少,并且能够缩短治疗时间,值得临床推广。
参考文献





